题目内容
【题目】根据要求回答下列问题:
(1)生活中明矾常作净水剂,其净水的原理是________________________(用离子方程式表示)。
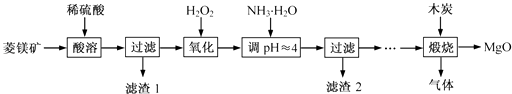
(2)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理________________________。
(3)去年8月12日晚,天津滨海新区危险品仓库发生爆炸事故,少量氰化物因爆炸冲击发生泄漏,CN一有剧毒,泄露会污染水源和空气,需要处理。
①已知HCN为一元弱酸,则NaCN溶液的pH _____________7(填“>”“=”或“<”),用离子方程式说明_____________________________。
②处理含CN一废水的方法之一是在微生物的作用下,CN-被氧气氧化成HCO3一,同时生成NH3,该反应的离子方程式为___________________________________________________。
(4)常温下,取0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合,测得溶液混合后的pH=5,写出MOH的电离方程式:____________________________________________。
【答案】 Al3+ +3H2O![]() Al(OH)3 + 3H+ MgO+2NH4Cl+H2O = MgCl2+2 NH3·H2O或NH4Cl+H2O
Al(OH)3 + 3H+ MgO+2NH4Cl+H2O = MgCl2+2 NH3·H2O或NH4Cl+H2O ![]() NH3·H2O+HCl,MgO+2HCl=MgCl2+H2O > CN-+H2O=HCN + OH- 2CN-+4H2O+O2=2HCO3- + 2NH3 MOH
NH3·H2O+HCl,MgO+2HCl=MgCl2+H2O > CN-+H2O=HCN + OH- 2CN-+4H2O+O2=2HCO3- + 2NH3 MOH![]() M++OH-
M++OH-
【解析】本题考查盐类的水解相关知识。(1)明矾溶于水电离出铝离子,铝离子易水解生成氢氧化铝胶体,胶体具有吸附性,能吸附水中的悬浮物而净水,所以明矾能净水,离子方程式为Al3+ +3H2O![]() Al(OH)3 + 3H+;(2)氯化铵溶液中铵根离子水解:NH4Cl+H2O
Al(OH)3 + 3H+;(2)氯化铵溶液中铵根离子水解:NH4Cl+H2O![]() NH3·H2O+HCl,溶液呈酸性,氧化镁和水解生成的盐酸反应生成氯化镁,方程式为:MgO+2NH4Cl+H2O = MgCl2+2 NH3·H2O或NH4Cl+H2O
NH3·H2O+HCl,溶液呈酸性,氧化镁和水解生成的盐酸反应生成氯化镁,方程式为:MgO+2NH4Cl+H2O = MgCl2+2 NH3·H2O或NH4Cl+H2O ![]() NH3·H2O+HCl,MgO+2HCl=MgCl2+H2O;(3)①HCN为一元弱酸,则NaCN为强碱弱酸盐,能发生水解:CN-+H2O
NH3·H2O+HCl,MgO+2HCl=MgCl2+H2O;(3)①HCN为一元弱酸,则NaCN为强碱弱酸盐,能发生水解:CN-+H2O![]() HCN + OH-,溶液呈碱性,故pH>7;②根据题中信息CN-被氧气氧化成HCO3一同时生成NH3,结合氧化还原反应配平即得:2CN-+4H2O+O2=2HCO3- + 2NH3;(4)常温下,取0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合,说明HCl与MOH的物质的量相等,二者恰好完全反应,生成MCl,测得溶液混合后的pH=5,说明MCl为强酸弱碱盐,能水解呈酸性,即MOH
HCN + OH-,溶液呈碱性,故pH>7;②根据题中信息CN-被氧气氧化成HCO3一同时生成NH3,结合氧化还原反应配平即得:2CN-+4H2O+O2=2HCO3- + 2NH3;(4)常温下,取0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合,说明HCl与MOH的物质的量相等,二者恰好完全反应,生成MCl,测得溶液混合后的pH=5,说明MCl为强酸弱碱盐,能水解呈酸性,即MOH![]() M++OH-。
M++OH-。