题目内容
19.下列溶液导电能力最强的是( )| A. | 0.1mol•L-1的氨水100mL | B. | 0.1mol•L-1的醋酸50mL | ||
| C. | 0.05mol•L-1的醋酸100mL | D. | 0.05mol•L-1的硫酸100mL |
分析 溶液的导电能力与溶液中离子所带电荷有关,根据各个选项中的离子所带电荷浓度的大小来回答,离子所带电荷浓度越大,导电能力最强.
解答 解:A、0.1mol/L氨水中一水合氨是弱电解质,部分电离,所以正电荷的浓度小于0.1mol/L
B、0.1mol/L醋酸中由于醋酸是弱电解质,部分电离,所以正电荷的浓度小于0.1mol/L;
C、醋酸是弱电解质,不完全电离,故0.05 mol/L醋酸,正电荷的浓度小于0.1mol/L;
D、0.05 mol/L硫酸中,正电荷的浓度为0.1 mol/L;
故选D.
点评 本题考查了溶液的导电能力与溶液中离子所带电荷有关,分析好各物质中离子所带电荷多少是解题的关键,难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
2.现有200.00mL含MgCl2和AlCl3的混合溶液,取20.00mL该溶液于锥形瓶中,用0.20mol•L-1标准硝酸银溶液滴定,滴几滴铬酸钾(K2CrO4)溶液作指示剂,滴定,至终点时消耗标准溶液25.00mL,另取100.00mL该溶液滴加过量氢氧化钠溶液,过滤、洗涤、灼烧、称重,得固体质量为0.2000g,原溶液中c(AlCl3)为( )
| A. | 0.05mol•L-1 | B. | 0.10mol•L-1 | C. | 0.30mol•L-1 | D. | 0.50mol•L-1 |
10.以下所含的化学键类型与晶体熔化需要破坏的作用力类型均相同的是( )
| A. | 干冰与水晶 | B. | 碘片和冰 | ||
| C. | 食盐和蔗糖 | D. | 氢氧化钠和五氧化二磷 |
7.下列各组内物质的转化,只通过一步反应不能完成的是( )
| A. | Zn→H2 | B. | CaO→CaSO4 | C. | CO2→CaCO3 | D. | Cu→Cu(OH)2 |
14.解决“白色污染”问题,下列做法不宜提倡的是( )
| A. | 将废弃塑料直接填埋 | B. | 对废弃塑料回收再利用 | ||
| C. | 用布袋代替塑料袋 | D. | 使用新型可降解塑料 |
11.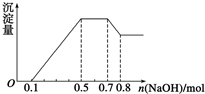 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A. | 溶液中的阳离子只有H+、Mg2+、Al3+ | |
| B. | 溶液中n(NH4+)=0.1mol | |
| C. | 溶液中一定不含CO32-,可能含有SO42-和NO3- | |
| D. | n(H+):n(Al3+):n(Mg2+)=2:2:1 |
8.化学与社会、生产、生活密切相关,下列说法正确的是( )
| A. | 乙醇和汽油都是可再生能源,应大力推广使用乙醇汽油 | |
| B. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| C. | 神舟飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 | |
| D. | “辽宁舰”上用于舰载机降落拦阻索的是一种特种钢缆,属于新型无机非金属材料 |
9.下列反应过程中,能量变化符合如图的是( )
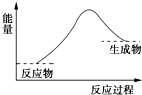

| A. | Zn与盐酸反应 | B. | CaO与H2O反应 | ||
| C. | NaOH溶液与盐酸反应 | D. | 消石灰与NH4Cl固体反应 |