��Ŀ����
����Ŀ���̷���FeSO47H2O����������ˮ�������ݼ��ȣ�ij�о�С��ⶨ��������պ����������Ҫ�ɷ֣�Fe2O3��Al2O3��SiO2 �� �������������ʣ��ĺ������Ʊ����̷����������£� 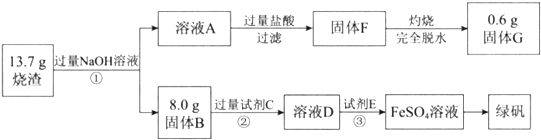
��ش��������⣺
��1����ҺA�к��е���������Ҫ��AlO2����SiO32���� ��
��2���Լ�C�� ��
��3�����з�Ӧ�����ӷ���ʽ�� ��
��4��������Fe2O3��Al2O3��SiO2�����ʵ���֮���� ��
���𰸡�
��1��OH��
��2��ϡ����
��3��Fe+2Fe3+=3Fe2+ �� Fe+2H+=Fe2++H2��
��4��5��5��1
���������⣺��1��ͨ�����Ϸ���֪����ҺA�к��е���������Ҫ��AlO2����SiO32����OH�� �� ���Դ��ǣ�OH������2��ͨ�����Ϸ���֪���Լ�C��ϡ���ᣬ���Դ��ǣ�ϡ�����3��ͨ�����Ϸ���֪�����з�Ӧ�����ӷ���ʽ��Fe+2Fe3+=3Fe2+��Fe+2H+=Fe2++H2�������Դ��ǣ�Fe+2Fe3+=3Fe2+��Fe+2H+=Fe2++H2������4��ͨ�����Ϸ���֪��SiO2Ϊ0.6g��Fe2O3Ϊ8.0g������Al2O3Ϊ13.7��8.0��0.6=5.1g����������Fe2O3��Al2O3��SiO2�����ʵ���֮���� ![]() ��
�� ![]() ��
�� ![]() =5��5��1�����Դ��ǣ�5��5��1��
=5��5��1�����Դ��ǣ�5��5��1��