题目内容
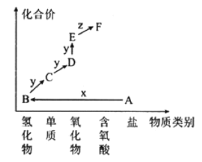
【题目】如图是元素M的价类二维图。其中A是一种盐,E的相对分子质量比D的相对分子质量大16,A和B是含最低价M元素的两种化合物,当x为一种强碱时,有如下转化关系。下列说法不正确的是( )
A.物质B遇少量的氯气会产生白烟
B.F的浓溶液可以用铁制容器盛放
C.E与水反应可生成F
D.物质D能够被x完全吸收
【答案】D
【解析】
A是一种盐,E的相对分子质量比D的相对分子质量大16,两者皆为氧化物,可初步判断E比D多一个氧原子。联想已构建的中学化学知识网络,符合这种转化关系的有:SO2→SO3,NO→NO2等。由此可出推断y为O2,由于F为酸,则E应为能转化为酸的某物质,很可能为SO3、NO2等。若E为NO2,顺推F为HNO3,Z为H2O,逆推D为NO,C为N2, B为NH3,A为铵盐。而X是强碱,A能与强碱生成B,综合而得A应为铵盐,B为NH3,C为N2,D为NO,E为NO2,F为HNO3,Z为H2O。
A.物质B为NH3,遇少量的氯气会生成NH4Cl,即产生白烟,A正确;
B.F的浓溶液为浓HNO3,铁与浓硝酸会发生钝化反应,所以浓硝酸可以用铁制容器盛放,B正确;
C.E为NO2,与水反应可生成F(HNO3),C正确;
D.物质D为NO,x为强碱,NO与x不反应,D错误;
答案选D。

【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 |
|
| HClO |
|
|
电离平衡常数 |
|
|
|
|
|
(1)25℃时,等浓度的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液,3种溶液的pH由大到小的顺序为________。
溶液,3种溶液的pH由大到小的顺序为________。
(2)工业上可用氨水除去尾气![]() 。将
。将![]() 通入氨水中,当
通入氨水中,当![]() 降至
降至![]() _____。
_____。
(3)常温下,用![]() 溶液滴定
溶液滴定![]() 溶液所得滴定曲线如图:
溶液所得滴定曲线如图:
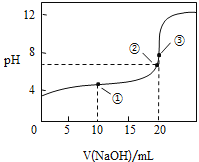
①在整个实验过程中,不需要的仪器或用品是 ______(填序号).
![]() 容量瓶 b 锥形瓶c 滴定管夹d 漏斗e 玻璃棒f 滴定管
容量瓶 b 锥形瓶c 滴定管夹d 漏斗e 玻璃棒f 滴定管
②到达滴定终点的标志是 _____________ .
③下列操作会导致测定结果偏高的是 ______ .
A 碱式滴定管在装液前未用标准NaOH溶液润洗
B 滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C 碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D 达到滴定终点时,仰视读数
④如图点①所示溶液中![]() __________
__________![]() 填“>”“<”或“=”,下同,点②所示溶液中:
填“>”“<”或“=”,下同,点②所示溶液中:![]() ________
________![]() ,点③所示溶液中所有离子浓度由大到小的顺序为:_________。
,点③所示溶液中所有离子浓度由大到小的顺序为:_________。
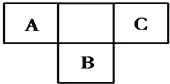
【题目】表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )
A | B | C | ||
D | ||||
A.原子半径大小比较为D>C>B>A
B.生成的氢化物分子间均可形成氢键
C.A与C形成的阴离子可能有AC![]() 、A2C
、A2C![]()
D.A、B、C、D的单质常温下均不导电