题目内容
(14分)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:

(1)此流程的第II步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
从上表可以推断:此反应是 (填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为 。
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是
A.2c1= c2 =c3 B.2Q1=Q2=Q3 C.α1 =α2 =α3 D.α1 +α2 ="1"
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是 。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
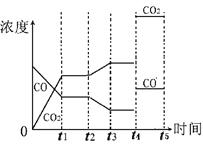
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是 、
(写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。

(1)此流程的第II步反应为:CO(g)+H2O(g)
 H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1[来源:] |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是 。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是 、
(写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。

(1)放;66.7%(2)AD (3)②③(4)降低温度,或增加水蒸汽的量,或减少氢气的量;(每格2分)

(1)温度越高,平衡常数越小,所以正反应是放热反应。
CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
起始量(mol) 1 2 0 0
转化量(mol) x x x x
平衡量(mol) 1-x 2-x x x
根据平衡常数知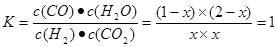
解得x=2/3,所以平衡后CO的转化率为是66.7%。
(2)因为反应前后体积,即改变压强平衡不会发生移动,根据所给的反应物投入量来看ABC就是等效的,虽然氢气的含量,但氢气的浓度不同,其中BC相等且都是A的2倍。根据500℃平衡常数可计算出A中反应物的转化率均是75%【计算方法同(1)】,即平衡时A中CO、H2O、H2、CO2分别是0.25mol、0.25mlol、0.75mol、0.75mol,则平衡时B、C中CO、H2O、H2、CO2分别都为0.5mol、0.5mol、1.5mol、1.5mol。即B、C中转化率分别是25%和75%。A中放热Q1,所以反应热是-2Q1kJ·mol-1。则C中放热2Q1,B中吸热Q1。答案AD正确。
(3)因为体系绝热,而反应是放热反应,所以压强会发生变化,①⑤可以。反应前后气体质量和容器的体积均不发生变化,所以密度不变,②不可以。反应前后气体质量和物质的量均不发生变化,所以相对分子质量不变,③不可以。④⑥符合化学平衡的概念正确。答案是②③。
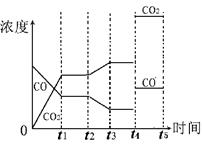
(4)由图像可知t2时刻CO浓度减小,CO2浓度增大,因此改变的条件是降低温度,或增加水蒸汽的量。t4时刻通过改变容积的方法将压强增大为原先的两倍,平衡不移动,但物质的浓度均增大,都变为原来大2倍,如图所示:
CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)起始量(mol) 1 2 0 0
转化量(mol) x x x x
平衡量(mol) 1-x 2-x x x
根据平衡常数知
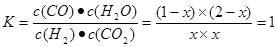
解得x=2/3,所以平衡后CO的转化率为是66.7%。
(2)因为反应前后体积,即改变压强平衡不会发生移动,根据所给的反应物投入量来看ABC就是等效的,虽然氢气的含量,但氢气的浓度不同,其中BC相等且都是A的2倍。根据500℃平衡常数可计算出A中反应物的转化率均是75%【计算方法同(1)】,即平衡时A中CO、H2O、H2、CO2分别是0.25mol、0.25mlol、0.75mol、0.75mol,则平衡时B、C中CO、H2O、H2、CO2分别都为0.5mol、0.5mol、1.5mol、1.5mol。即B、C中转化率分别是25%和75%。A中放热Q1,所以反应热是-2Q1kJ·mol-1。则C中放热2Q1,B中吸热Q1。答案AD正确。
(3)因为体系绝热,而反应是放热反应,所以压强会发生变化,①⑤可以。反应前后气体质量和容器的体积均不发生变化,所以密度不变,②不可以。反应前后气体质量和物质的量均不发生变化,所以相对分子质量不变,③不可以。④⑥符合化学平衡的概念正确。答案是②③。
(4)由图像可知t2时刻CO浓度减小,CO2浓度增大,因此改变的条件是降低温度,或增加水蒸汽的量。t4时刻通过改变容积的方法将压强增大为原先的两倍,平衡不移动,但物质的浓度均增大,都变为原来大2倍,如图所示:


练习册系列答案
相关题目
 H2+I2
H2+I2
 2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变
2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变 (g)+
(g)+ 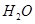 (g)=
(g)=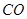 (g)+
(g)+ (g)
(g) 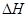 = +
= +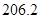
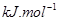
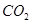 (g)=
(g)=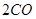 (g)+
(g)+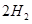 (g)
(g)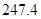
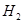 (g)的热化学方程式为 。
(g)的热化学方程式为 。 O的热分解也可得到H
O的热分解也可得到H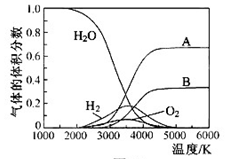
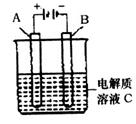
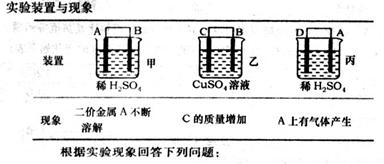
 N2(g
N2(g )+O2(g)
)+O2(g) 2NO(g) △H=a kJ·mol-1的平衡常数K如下表:
2NO(g) △H=a kJ·mol-1的平衡常数K如下表:
 2NH3。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
2NH3。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
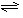 2NH3(g) △H = -92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
2NH3(g) △H = -92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
 WI2(g)。为模拟上述反应,准确称取0.508g碘、0.736g金属钨置于50.0mL的密闭容器中,加热使其反应。如图是WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1。则:①该反应的△H 0(填“大于”
WI2(g)。为模拟上述反应,准确称取0.508g碘、0.736g金属钨置于50.0mL的密闭容器中,加热使其反应。如图是WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1。则:①该反应的△H 0(填“大于”
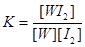




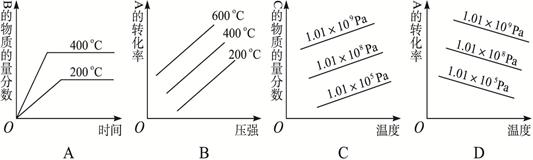
 2C(g)+Q (Q>0),下列图象正确的是 ?
2C(g)+Q (Q>0),下列图象正确的是 ?