题目内容
根据已知条件,对物质的性质强弱判断不正确的是( )
A.已知2C+SiO2
| ||||
| B.已知相同条件下气态氢化物的稳定性.HA>HB,说明还原性:A-<B- | ||||
C.已知 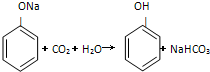 ,说明酸性:碳酸>苯酚 | ||||
| D.已知物质的量浓度相同的MCl和NCl两种溶液中c(M+)>c(N+),说明碱性:MOH>NOH |
A.2C+SiO2
Si+2CO↑,反应能进行的主要原因是生成了气体CO分离出原体系,只能说明碳易与氧结合,故A错误;
B.根据气态氢化物的稳定性HA>HB,可知A的非金属性大于B,故还原性:A-<B-,故B正确;
C.则根据强酸制弱酸的原理,碳酸的酸性比苯酚强,故C正确;
D.根据c(M+)>c(N+)可以推出,至少N+是会水解的(M+也可能水解,但是它的水解程度比N+小),因为一种阳离子,它的对应碱的碱性越弱,这种离子的水解能力就越强,等浓度时,水解程度就越大,所以可以知道有以下两种可能:1、M+不水解,那么MOH就是强碱,N+会水解,NOH就是弱碱;2、M+也水解,但是它的水解程度比N+小,那么MOH就是碱性比NOH略强的弱碱.总之,都可以得出碱性:MOH>NOH,故D正确.
故选A.
| ||
B.根据气态氢化物的稳定性HA>HB,可知A的非金属性大于B,故还原性:A-<B-,故B正确;
C.则根据强酸制弱酸的原理,碳酸的酸性比苯酚强,故C正确;
D.根据c(M+)>c(N+)可以推出,至少N+是会水解的(M+也可能水解,但是它的水解程度比N+小),因为一种阳离子,它的对应碱的碱性越弱,这种离子的水解能力就越强,等浓度时,水解程度就越大,所以可以知道有以下两种可能:1、M+不水解,那么MOH就是强碱,N+会水解,NOH就是弱碱;2、M+也水解,但是它的水解程度比N+小,那么MOH就是碱性比NOH略强的弱碱.总之,都可以得出碱性:MOH>NOH,故D正确.
故选A.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
根据已知条件,对物质的性质强弱判断不正确的是( )
| A、已知HF的共价键键能比HCl大,说明稳定性:HF>HCl | ||||
| B、已知正反应的活化能大于逆反应的活化能,说明总能量:生成物>反应物 | ||||
C、已知 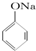 +SO2+H2O→ +SO2+H2O→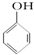 +Na2SO3,说明给出质子能力:HSO3->苯酚 +Na2SO3,说明给出质子能力:HSO3->苯酚 | ||||
D、已知CaCO3+SiO2
|

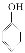

 Si+2CO↑,说明非金属性:碳>硅
Si+2CO↑,说明非金属性:碳>硅 ,说明酸性:碳酸>苯酚
,说明酸性:碳酸>苯酚