题目内容
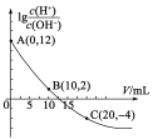
【题目】25℃时,用0.10mol·L的氨水滴定l0.00mL0.05mol·L-1H2A溶液,加入氨水的体积(V)与溶液中lg![]() 的关系如图所示(忽略溶液体积变化)。下列说法不正确的是
的关系如图所示(忽略溶液体积变化)。下列说法不正确的是
A.A点溶液的pH等于1
B.由图中数据可知,H2A为弱酸
C.B点水电离出的H+离子浓度为1.0×10-6mol·L-1
D.C点溶液中![]()
【答案】B
【解析】
A点:根据c(H+)×c(OH-)=KW=1×10-14,lg![]() =12,计算得c(H+)=10-1mol/L,则pH=1,同时可知0.05mol·L-1H2A完全电离为强酸;B点:酸碱恰好完全中和生成盐(NH4)2A的点,根据lg
=12,计算得c(H+)=10-1mol/L,则pH=1,同时可知0.05mol·L-1H2A完全电离为强酸;B点:酸碱恰好完全中和生成盐(NH4)2A的点,根据lg![]() =2,c(H+)×c(OH-)=KW=1×10-14计算得c(H+)=10-6mol/L;C点:(NH4)2A与氨水混合物,根据lg
=2,c(H+)×c(OH-)=KW=1×10-14计算得c(H+)=10-6mol/L;C点:(NH4)2A与氨水混合物,根据lg![]() =-4,c(H+)×c(OH-)=KW=1×10-14,计算得c(H+)=10-9mol/L,则pH=9,偏碱性,考虑氨水的电离平衡,以此进行分析。
=-4,c(H+)×c(OH-)=KW=1×10-14,计算得c(H+)=10-9mol/L,则pH=9,偏碱性,考虑氨水的电离平衡,以此进行分析。
A. A点:根据c(H+)×c(OH-)=KW=1×10-14,lg![]() =12,计算得c(H+)=10-1mol/L,则pH=1,故不选A;
=12,计算得c(H+)=10-1mol/L,则pH=1,故不选A;
B. 根据A点:c(H+)×c(OH-)=KW=1×10-14,lg![]() =12,计算得c(H+)=10-1mol/L,得0.05mol/LH2A完全电离,H2A为强酸,故选B;
=12,计算得c(H+)=10-1mol/L,得0.05mol/LH2A完全电离,H2A为强酸,故选B;
C. B点酸碱恰好完全中和生成盐(NH4)2A的点,lg![]() =2,计算得c(H+)=10-6mol/L,则水电离出的H+离子浓度为1.0×10-6mol·L-1,故不选C;
=2,计算得c(H+)=10-6mol/L,则水电离出的H+离子浓度为1.0×10-6mol·L-1,故不选C;
D. C点NH4)2A与氨水混合物,根据lg![]() =-4,计算得c(H+)=10-9mol/L,则pH=9,偏碱性,考虑氨水的电离平衡,则溶液中
=-4,计算得c(H+)=10-9mol/L,则pH=9,偏碱性,考虑氨水的电离平衡,则溶液中![]() ,故不选D;
,故不选D;
答案:B

练习册系列答案
相关题目