��Ŀ����
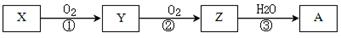
ij�о���ѧϰС��ͨ������ʵ��̽��SO2�ܷ���BaCl2��Һ��Ӧ����BaSO3���������Ʊ�����ͭ���塣���������ա���ͬѧ��װ��I����ʵ�飬���ȷ�Ӧ�������ڣ�����BaCl2��Һ�г��ְ�ɫ�������Ұ�ɫ�������������ᡣ

��1����ɫ������ ��
��2����ͬѧ�Ͱ�ɫ����������ԭ����������ּ��裬�����ּ�������ǣ�
�� ��
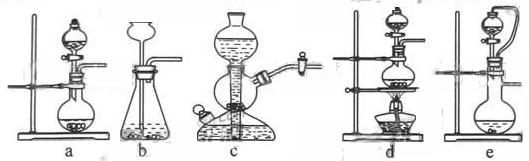
��ͬѧ����˸Ľ�װ�â����ʵ�飬�����ͬѧ����ļ��裨�г�װ�ú�A�м���װ�����ԣ��������Ѽ��飩��
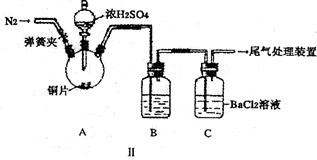
�ٴ��ɼУ�ͨ��N2һ��ʱ���رյ��ɼУ�
�ڵμ�һ����Ũ���ᣬ����A��һ��ʱ���C��δ���������ɡ�
��3�������ٵ�Ŀ���� ������ƿB�е��Լ��� ��
��4����ʵ���ܷ�����ͬѧ�������ּ����е�����һ�� �������� ��
��ͬѧ��Ӧ�����ɫ��Һ�м���������CuO�����˺���Һ�Ƴ�����ͭ���壨CuSO4��xH2O�������ü��ȷ��ⶨ�þ����нᾧˮx��ֵ��ʵ�����ݼ�¼���£�
��5���������ٽ��е����γ�������a����ֵ��ΧӦΪ ��
��6�������Ⱥ����������������Ϊ18.620g������x ��ʵ��ֵ ��������λС������������ ��

��1����ɫ������ ��
��2����ͬѧ�Ͱ�ɫ����������ԭ����������ּ��裬�����ּ�������ǣ�
�� ��
��ͬѧ����˸Ľ�װ�â����ʵ�飬�����ͬѧ����ļ��裨�г�װ�ú�A�м���װ�����ԣ��������Ѽ��飩��

�ٴ��ɼУ�ͨ��N2һ��ʱ���رյ��ɼУ�
�ڵμ�һ����Ũ���ᣬ����A��һ��ʱ���C��δ���������ɡ�
��3�������ٵ�Ŀ���� ������ƿB�е��Լ��� ��
��4����ʵ���ܷ�����ͬѧ�������ּ����е�����һ�� �������� ��
��ͬѧ��Ӧ�����ɫ��Һ�м���������CuO�����˺���Һ�Ƴ�����ͭ���壨CuSO4��xH2O�������ü��ȷ��ⶨ�þ����нᾧˮx��ֵ��ʵ�����ݼ�¼���£�
| �������� | �����뾧�������� | ���Ⱥ���������������� | |
| ��һ�γ��� | �ڶ��γ��� | ||
| 11.710g | 22.700g | 18.621g | a |
��5���������ٽ��е����γ�������a����ֵ��ΧӦΪ ��
��6�������Ⱥ����������������Ϊ18.620g������x ��ʵ��ֵ ��������λС������������ ��
��1��BaSO4��2�֣���
��2����Ũ����������������Ȼ�����Һ���ɳ�����1�֣�
��SO2�������������������ɳ�����1�֣�
��3���ų�װ���ڵĿ�����O2����1�֣� ����NaHSO3��Һ��1�֣�
��4�����ܣ�1�֣�����Ϊͬʱ�ı���������������ȷ���������ĸ����������á���1�֣�
��5��18.621��0.001 ��1�֣�
��6��5.25 ��2�֣� +5%��1�֣�
��2����Ũ����������������Ȼ�����Һ���ɳ�����1�֣�
��SO2�������������������ɳ�����1�֣�
��3���ų�װ���ڵĿ�����O2����1�֣� ����NaHSO3��Һ��1�֣�
��4�����ܣ�1�֣�����Ϊͬʱ�ı���������������ȷ���������ĸ����������á���1�֣�
��5��18.621��0.001 ��1�֣�
��6��5.25 ��2�֣� +5%��1�֣�
�����������1����ɫ�������������ᣬ��˰�ɫ���������ᱵ��
��2����������ķе�ͼ����¶ȷ�����˵��Ũ�������¶Ƚϸ�ʱҲ�ܻӷ���H2SO4����������BaSO3�ܹ��������ᣬ����Ԫ���غ��֪�ó���ֻ����BaSO4���п���һ�ǻӷ�����H2SO4�ṩ��SO42-��Ba2+��Ӧ���ɵģ�Ҳ�п�������Һ���ܽ��������SO2���ò��������ᣬ�����õ�BaSO4��
��3�����������ȶ����ž�װ���еĿ����е�����������֤����ԭ���Ƿ���ȷ��Ϊ��ȥ��Ӧ�д�������״���ᣬ���Խ�����ͨ������NaHSO3��Һ��
��4������ͬʱ�ı���������������ȷ���������ĸ����������á�
��5����������ʵ�����ܳ���0.001�������������ٽ��е����γ�������a����ֵ��ΧӦΪ18.621��0.001��
��6�������Ⱥ����������������Ϊ18.620g�����ʧȥ�Ľᾧˮ����Ϊ22.700g ��18.620g��4.08g��ˮ�����ʵ�����0.227mol�����������Ϊ22.700g��11.710g��10.99g����
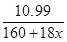 ��x��0.227
��x��0.227���x��5.25�����������Ϊ
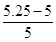 ��100%��5%��
��100%��5%��
��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
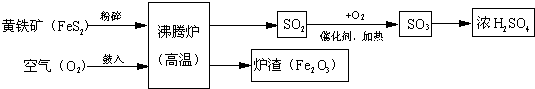



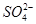 ʱ��Ӧȡ��������Һ�����μ���BaCl2��Һ��ϡ����
ʱ��Ӧȡ��������Һ�����μ���BaCl2��Һ��ϡ����