��Ŀ����
����Ŀ����ش��ȼҵ���������⣺
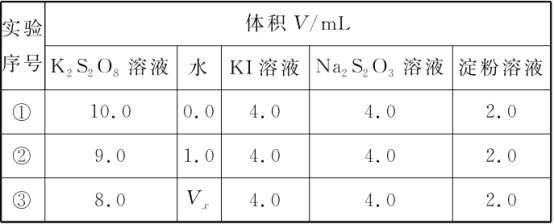
��1���������ռ��ǵ��ʳ��ˮʱ���չ̶��ı���k�������ȣ����ɵIJ�Ʒ��������k��_______��Ҫ��������ʽ�ͽ������
��2��ԭ�ϴ����г�������ɳ��Ca2����Mg2����Fe3����SO42�������ʣ����뾫�ƺ���ܹ����ʹ�á�����ʱ����������ˮ���˺�Ҫ������Լ��ֱ�Ϊ��Na2CO3����HCl�����ᣩ��BaCl2����3���Լ����ӵĺ���˳����______________������ţ���
��3���ȼҵ�Ǹߺ��ܲ�ҵ��һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����
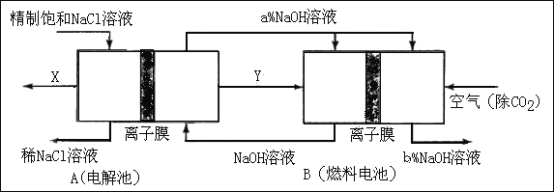
��ͼ��X��Y�ֱ���_____��_______���ѧʽ���������Ƚ�ͼʾ������������������a����b���Ĵ�С_________��
�ڷֱ�д��ȼ�ϵ��B�������������Ϸ����ĵ缫��Ӧ������______��������_____��
��������Ƶ���Ҫ�ڣ��磩��֮�����ڣ�д��2����____________��____________��
���𰸡�M(Cl2)/[2 M(NaOH)]=71/80=1:1.13��0.89 �ۢ٢� Cl2 H2 a%С��b% O2+4e-+2H2O��4OH- H2��2e-+2OH-��2H2O ȼ�ϵ�ؿ��Բ���������ĵĵ��ܣ������ܺ� ��߲�����Һ��Ũ��
��������
��1�����ʳ��ˮ�Ļ�ѧ����ʽΪ2NaCl��2H2O![]() 2NaOH��H2����Cl2��������k=M��Cl2��/[2M��NaOH��]=71/80=1:1.13=0.89��
2NaOH��H2����Cl2��������k=M��Cl2��/[2M��NaOH��]=71/80=1:1.13=0.89��
��2�����ڼ���ij����Լ������������ij����Լ����Ϊ�����ʣ����Թ����ij����Լ�Ҳ�����ȥ����Na2CO3����BaCl2֮��Na2CO3�������ڳ�ȥCa2+�����ҳ�ȥ������Ba2��������BaCl2��Na2CO3���˳�ȥ�����Ȼ����������ȥ������CO32-��3���Լ����ӵĺ���˳���Ǣۢ٢ڡ�
��3����ȼ�ϵ����ͨ����(������)��һ��ӦΪ����������Y(ͨ�븺������ԭ��)��ΪH2����A�����أ���H2�����ڵ��ص�������������ڵ���������X��ΪCl2��a% NaOH��Һ����ȼ�ϵ�أ�ȼ�ϵ�ص�������ӦʽΪO2��4e����2H2O=4OH����ˮ���١�OH�����࣬Na+ͨ������Ĥ�������ƶ�����ȼ�ϵ������������NaOH��Һ�����������a%<b%��
��ȼ�ϵ��B��������ӦʽΪO2��4e����2H2O=4OH���������缫��ӦʽΪ2H2-4e-+4OH-=4H2O��
��������Ƶ���Ҫ�ڣ��磩��֮�����ڣ�ȼ�ϵ�ؿ��Բ���������ĵĵ��ܣ������ܺģ���߲�����Һ��Ũ�ȡ�

����Ŀ�����������л����ش��������⣺
A�� | B�� | C�� |
D��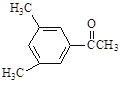 E��
E��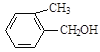 F��
F��![]()
��1��A�����к��еĹ���������Ϊ_____________��______________��
��2��B�ķ���ʽΪ_________________��
��3��D��һ�ȴ��������________________�֡�
��4�������������л�Ϊͬ���칹�����_____����Ϊͬϵ�����____��������ĸ��