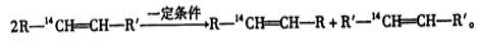��Ŀ����
��17�֣���2012?�㶫��������㷺Ӧ������ҩ�ͻ�����ҵ��ijͬѧ�����üױ���������Ӧ�Ʊ������ᣬ��Ӧԭ����
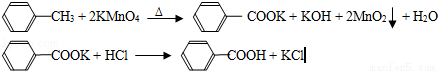
ʵ�鷽����һ�����ļױ���KMnO4��Һ��100����Ӧһ��ʱ���ֹͣ��Ӧ�����������̷����������ͻ���δ��Ӧ�ļױ���
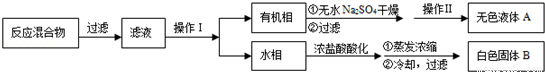
��֪�������������122���۵�122.4������25����95��ʱ�ܽ�ȷֱ�Ϊ0.3g��6.9g�����������л��ﶼ�й̶��۵㣮
��1���������� ������������ ����
��2����ɫҺ��A���� �������Լ���A���Լ����� ������������
��3���ⶨ��ɫ����B���۵㣬��������115����ʼ�ۻ����ﵽ130��ʱ�����������ۣ���ͬѧ�Ʋ��ɫ����B�DZ�������KCl�Ļ�����������·��������ᴿ�ͼ��飬ʵ���������Ʋ���ȷ�����ڴ������ɱ������ݣ�
��� | ʵ�鷽�� | ʵ������ | ���� |
�� | ����ɫ����B����ˮ�У������ܽ⣬��_________�� ��_________�� | �õ���ɫ�������ɫ��Һ |
|
�� | ȡ������Һ���Թ��У���_________�� | ���ɰ�ɫ���� | ��Һ��Cl�� |
�� | �����ɫ���壬��_________�� | ��_________�� | ��ɫ�����DZ����� |
��4�����Ȳⶨ����ȡ1.220g��Ʒ�����100ml�״���Һ����ȡ25.00ml��Һ���ζ�������KOH�����ʵ���Ϊ2.40��10��3mol����Ʒ�б��������������ļ������ʽΪ�� ����������Ϊ�� ����������λ��Ч���֣���
��1����Һ������2������KMnO4��Һ����ɫ��Һ��ɫ��3��
��� | ʵ�鷽�� | ʵ������ |
���� |
�� | ����ɫ����B����ˮ�У����ȣ��ܽ⣬��ȴ������ | �õ���ɫ�������ɫ��Һ |
|
�� | ȡ������Һ���Թ��У����������������ữ��AgNO3��Һ | ���ɰ�ɫ���� | ��Һ����Cl�� |
�� | �����ɫ���壬����ʹ���ڻ��������۵㣻 | �۵�Ϊ122.4�� | ��ɫ�����DZ����� |
��4��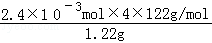 ��100%�� 96%
��100%�� 96%
����������1���������̷������������ʵ�鷽���Ͳ������裻
��2�����ݷ����Լ����̿�֪���л�������Ҫ��Ϊ��Ӧ�ļױ����ױ��DZ���ͬϵ����Ա����������Һ������
��3����Ϸ�Ӧ��ѧ����ʽ�����ɵIJ���������з��벽���������ɫ����B�DZ�������KCl�Ļ������ݱ������۵�122.4������25����95��ʱ�ܽ�ȷֱ�Ϊ0.3g��6.9g���ȼ��鱽����ļ����ټ����Ȼ��صĴ��ڣ�
��������
��1��һ�����ļױ���KMnO4��Һ��100����Ӧһ��ʱ���ֹͣ��Ӧ�������̷����������ͻ���δ��Ӧ�ļױ������Բ������Ƿ�����л���ױ����÷�Һ�����õ���������������ķ������Ƽױ��е�õ������ļױ�Һ�壻�ʴ�Ϊ����Һ������
��2���������̺��ƶϿ�֪����ɫҺ��AΪ�ױ��������Լ����������Ը��������Һ���ױ�������Ϊ�����ᣬ���������Һ��ɫ��ȥ��
�ʴ�Ϊ������KMnO4��Һ����ɫ��Һ��ɫ��
��3��ͨ���ⶨ��ɫ����B���۵㣬��������115����ʼ�ۻ����ﵽ130��ʱ�����������ۣ��Ʋ��ɫ����B�DZ�������KCl�Ļ����Ȼ��ؿ����������ữ����������Һ���������ӵĴ��ڣ����ñ�������ܽ��������25����95��ʱ�ܽ�ȷֱ�Ϊ0.3g��6.9g�����ò�ͬ�¶��µ��ܽ�ȣ���������õ������ͨ���ⶨ�۵��ж��Ƿ�Ϊ�����
�ʴ�Ϊ��
��� | ʵ�鷽�� | ʵ������ |
���� |
�� | ����ɫ����B����ˮ�У����ȣ��ܽ⣬��ȴ������ | �õ���ɫ�������ɫ��Һ |
|
�� | ȡ������Һ���Թ��У����������������ữ��AgNO3��Һ | ���ɰ�ɫ���� | ��Һ����Cl�� |
�� | �����ɫ���壬����ʹ���ڻ��������۵㣻 | �۵�Ϊ122.4�� | ��ɫ�����DZ����� |
��4����ȡ1.220g��Ʒ�����100ml�״���Һ����ȡ25.00ml��Һ���ζ�������KOH�����ʵ���Ϊ2.40��10��3mol����������һԪ�������������1��1��Ӧ���������ʵ�����ͬ��ע����Һ����仯������Ʒ�� ����������ʵ���������������������Ʒ�б�������������=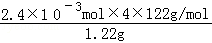 ��100%=96%��
��100%=96%��
�ʴ�Ϊ��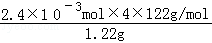 ��100%�� 96%
��100%�� 96%

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�