题目内容
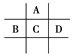
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1 mol E单质与足量酸作用,在标准状况下能产生33.6 L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
(1)A与E形成化合物的化学式是_____。
(2)B的最高价氧化物化学式为_______,C的元素名称为______,D的单质与水反应的方程式为_______。
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现是____,有关反应的离子方程式为________。
【答案】Al2O3 P2O5 硫 Cl2+H2O![]() HCl+HClO 先有白色胶状沉淀产生并逐渐增多,随NaOH溶液的加入又逐渐溶解最终澄清 Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O
HCl+HClO 先有白色胶状沉淀产生并逐渐增多,随NaOH溶液的加入又逐渐溶解最终澄清 Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O
【解析】
根据原子结构及元素周期表的结构推测元素的种类,根据元素性质分析解答。
设A的原子序数为x,则同主族的元素C原子序数为x+8,与C同周期的元素B原子序数为x+7,D的原子序数为x+9,则x+(x+8)+(x+7)+(x+9)=56,则x=8,则A为氧,B为磷,C为硫,D为氯;1molE置换出H2的物质的量为33.6L/22.4L/mol=1.5mol/L,根据电子转移守恒推测1molE失去3mol电子,E的阳离子与A的阴离子核外电子层结构完全相同,则E为铝;
(1)A为O,E为Al,形成化合物的化学式是Al2O3;
(2)B为P,最外层电子数为5,则其最高价氧化物化学式为P2O5;C为S,元素名称为硫;D为氯,氯气与水反应的方程式为 Cl2+H2O![]() HCl+HClO;
HCl+HClO;
(3)D与E形成的化合物为AlCl3,氯化铝溶液与氢氧化钠溶液反应先生成氢氧化铝沉淀,氢氧化铝为两性,又与氢氧化钠溶液反应生成偏铝酸钠,所以观察到的现是先有白色胶状沉淀产生并逐渐增多,随NaOH溶液的加入又逐渐溶解最终澄清;有关反应的离子方程式为Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O。

【题目】恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2L的恒容密闭容器中发生反应:2SO2(g)+O2(g) ![]() 2SO3(g) (正反应为放热反应),SO2的物质的量随时间变化的关系如表所示:
2SO3(g) (正反应为放热反应),SO2的物质的量随时间变化的关系如表所示:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
下列说法错误的是
A. 4~5min内,该反应的正、逆反应速率相等
B. 若要提高SO3的产率,则可用过量的空气代替O2
C. 从反应开始到达到平衡,用SO3表示的平均反应速率为0.015mol/ (L·min)
D. 容器内反应达到平衡状态时的压强与起始时的压强之比为5∶4