题目内容
【题目】前几年我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2 , X原子的结构示意图为 ![]() ,X的阳离子与Y的阴离子的电子层结构相同.元素Z,W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z,W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z,W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z,W能形成一种WZ2型分子.
(1)m= , 该融雪剂的化学式为 . 用电子式表示该融雪剂微粒的形成过程: .
(2)Z,W元素的名称为、 .
(3)下列说法正确的是 .
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是 .
A.XY2的电子式:X2+[ ![]()
![]()
![]()
![]()
![]() ]2﹣
]2﹣
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2﹣═2Y+Z↓
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因 .
【答案】
(1)20;CaCl2;![]()
(2)硫;碳
(3)B
(4)B
(5)水分子之间存在氢键
【解析】解:X原子的结构示意图为 ![]() ,由于K最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,故X为Ca元素;由化学XY2可知Y的化合价为﹣1价,而X的阳离子与Y的阴离子的电子层结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl,则该融雪剂为CaCl2;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2 . (1)由上述分析可知,m=2+8+8+2=20,该融雪剂的化学式为CaCl2 , 用电子式表示氯化钙的形成过程:
,由于K最多容纳2个电子,L层最多容纳8个电子,可知a=2,b=8,故X为Ca元素;由化学XY2可知Y的化合价为﹣1价,而X的阳离子与Y的阴离子的电子层结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl,则该融雪剂为CaCl2;元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,符合条件的元素有He、C、S,由于Z与Y相邻且Z、W能形成一种WZ2型分子,则Z为S元素,W为C元素,二者形成的分子为CS2 . (1)由上述分析可知,m=2+8+8+2=20,该融雪剂的化学式为CaCl2 , 用电子式表示氯化钙的形成过程: ![]() ,所以答案是:20;CaCl2;
,所以答案是:20;CaCl2; ![]() ;(2)由上述分析可知,Z为硫元素、W为碳元素,所以答案是:硫;碳;(3)A.CaCl2属于离子化合物,而CS2是共价化合物,故A错误; B.CaCl2中仅含离子键,CS2中只含共价键,且是极性共价键,故B正确; C.因氯的非金属性强于硫,所以稳定性HCl>H2S,故C错误; D.核外电子排布相同的离子,核电荷数越大,离子的半径越小,所以半径Ca2+<Cl﹣ , 故D错误,故选:B;(4)A.CaCl2为离子化合物,电子式为:
;(2)由上述分析可知,Z为硫元素、W为碳元素,所以答案是:硫;碳;(3)A.CaCl2属于离子化合物,而CS2是共价化合物,故A错误; B.CaCl2中仅含离子键,CS2中只含共价键,且是极性共价键,故B正确; C.因氯的非金属性强于硫,所以稳定性HCl>H2S,故C错误; D.核外电子排布相同的离子,核电荷数越大,离子的半径越小,所以半径Ca2+<Cl﹣ , 故D错误,故选:B;(4)A.CaCl2为离子化合物,电子式为: ![]() ,故A错误; B.CS2是直线形分子,结构式为S=C=S,故B正确; C.Cl2与H2S水溶液反应的离子方程式为:Cl2+H2S═2H++2Cl﹣+S↓,故C错误,故选:B;(5)冰雪的化学成分是H2O,水的沸点比H2S的沸点高,是由于水分子之间存在氢键,所以答案是:水分子之间存在氢键.
,故A错误; B.CS2是直线形分子,结构式为S=C=S,故B正确; C.Cl2与H2S水溶液反应的离子方程式为:Cl2+H2S═2H++2Cl﹣+S↓,故C错误,故选:B;(5)冰雪的化学成分是H2O,水的沸点比H2S的沸点高,是由于水分子之间存在氢键,所以答案是:水分子之间存在氢键.

【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中。“硫酸法”生产钛的原料是钛铁矿[主要成分是钛酸亚铁(FeTiO3),含有Fe(Ⅲ)等杂质],同时获得副产品甲的工业生产流程如下:
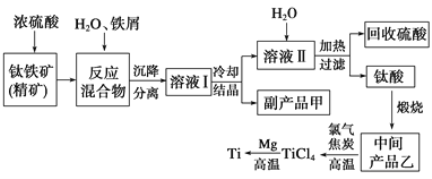
(1)浓硫酸处理钛铁矿时产物之一是TiOSO4,反应中无气体放出,写出该反应的化学方程式___。
(2)上述生产流程中加入铁屑的目的是_______________,可循环利用的物质是_________,检验副产品甲是否变质的实验方法是_________________________________。
(3)溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当pH等于_________时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该沉淀是_______________________________________。
(4)中间产品乙是一种氧化物,其经高温与氯气、焦炭反应,除生成TiCl4外,还生成了一种可燃性气体,请写出该反应的化学方程式___________。
(5)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还原控制的反应条件是__________________________________,反应后的产物需要加入______________溶解后才能达到提纯金属钛的目的。