题目内容
【题目】(14分)发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g)![]() CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H________(填“增大”、“减小”或“不变”),判断的理由是________。
CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H________(填“增大”、“减小”或“不变”),判断的理由是________。
(2)CO2制备甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH=-49.0kJ·mol-1,在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如右图所示。
CH3OH(g)+H2O(g)ΔH=-49.0kJ·mol-1,在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如右图所示。
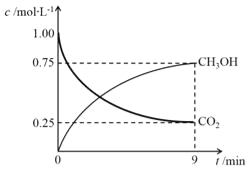
①该反应化学平衡常数K的表达式是________。
②0~9min时间内,该反应的平均反应速率ν(H2)=________。
③在相同条件下,密闭容器的体积缩小至0.5L时,此反应达平衡时放出的热量(Q)可能是________(填字母序号)kJ。
a.0<Q<29.5
B.29.5<Q<36.75
C.36.75<Q<49
D.49<Q<98
④在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如右图所示,L和X分别表示温度或压强。
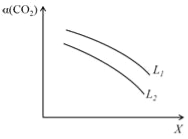
X表示的物理量是。判断L1与L2的大小关系。
(3)科学家用氮化镓材料与铜组装如右图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.
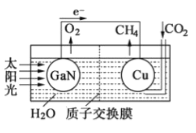
写出铜电极表面的电极反应式,为提高该人工光合系统的工作效率,可向装置中加入少量(选填“盐酸”或“硫酸”).
(4)利用CO2和NH3为原料也合成尿素,在合成塔中的主要反应可表示如下:
反应①:2NH3(g)+CO2(g)=NH2CO2NH4(s)△H1=__________________
反应②:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H2=+72.49kJ·mol-1
总反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-86.98kJ·mol-1;
则反应①的△H1=_______________。
(5)现将amol铁和bmol铜的混合物与含有cmolHNO3的稀溶液充分反应,设还原产物为NO。下列结论不正确的是(填序号)
A.若剩余金属0.5amol,则氧化产物为一种或二种
B.若只有一种氧化产物,则3c=8a
C.若有二种氧化产物,被还原的硝酸物质的量为0.25cmol
D.若有三种氧化产物,被还原的硝酸物质的量为0.25cmol
【答案】(1)不变(2)①0.25mol·L-1·min-1②c③温度L1>L2
(3)CO2+8H++8e-=CH4+2H2O硫酸;
(4)-159.47kJ/mol(5)BC
【解析】
试题分析:(1)将煤转化成水煤气的反应:C(s)+H2O![]() CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),催化剂改变反应速率不改变化学平衡,不改变反应焓变,此反应的△H不变;
CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),催化剂改变反应速率不改变化学平衡,不改变反应焓变,此反应的△H不变;
(2)①依据图像读取甲醇生成浓度,结合反应速率概念计算甲醇的反应速率=0.75mol/L÷9min,反应速率之比等于化学方程式计量数之比,V(H2)=3V(CH3OH(g)=3×0.75mol/L/9min=0.25mol/(Lmin);
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJmol-1,反应达到平衡状态消耗二氧化碳物质的量浓度=1mol/L-0.25mol/L=0.75mol/L,物质的量为0.75mol,反应放出热量=49kJ/mol×0.75mol=36.75kJ,反应焓变是指1mol二氧化碳和3mol氢气完全反应放出的热量为49kJ,反应是可逆反应,在体积为1L的密闭容器中,充入1molCO2和3molH2,反应放热一定小于49kJ,在相同条件下,密闭容器的体积缩小至0.5L时,压强增大,平衡正向进行,反应放出热量会增多,大于36.75kJ,则36.75<Q<49,答案选c;③CO2(g)+3H2(g)
CH3OH(g)+H2O(g)△H=-49.0kJmol-1,反应达到平衡状态消耗二氧化碳物质的量浓度=1mol/L-0.25mol/L=0.75mol/L,物质的量为0.75mol,反应放出热量=49kJ/mol×0.75mol=36.75kJ,反应焓变是指1mol二氧化碳和3mol氢气完全反应放出的热量为49kJ,反应是可逆反应,在体积为1L的密闭容器中,充入1molCO2和3molH2,反应放热一定小于49kJ,在相同条件下,密闭容器的体积缩小至0.5L时,压强增大,平衡正向进行,反应放出热量会增多,大于36.75kJ,则36.75<Q<49,答案选c;③CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJmol-1,反应是气体体积减小的放热反应,i.温度升高,平衡逆向进行,二氧化碳转化率减小,所以X为温度,L为压强;ii.温度一定压强增大平衡正向进行二氧化碳转化率增大,所以L1>L2;
CH3OH(g)+H2O(g)△H=-49.0kJmol-1,反应是气体体积减小的放热反应,i.温度升高,平衡逆向进行,二氧化碳转化率减小,所以X为温度,L为压强;ii.温度一定压强增大平衡正向进行二氧化碳转化率增大,所以L1>L2;
(3)根据电子的流向可知铜电极是正极,CO2得到电子转化为甲烷,则正极反应式为CO2+8H++8e-=CH4+2H2O;由于盐酸易挥发,生成的甲烷中会混有HCl气体,所以选用硫酸,不用盐酸;
(4)已知:反应②:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H2=+72.49kJ·mol-1
③:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-86.98kJ·mol-1
则根据盖斯定律可知③-②即得到反应①:2NH3(g)+CO2(g)=NH2CO2NH4(s)的△H1=-159.47kJ/mol;
(5)A、若剩余金属0.5amol,该金属可能为铁或铜,若为铁,则溶质为硝酸亚铁,若为铜,则氧化产物可能为硝酸亚铁和硝酸铜,A正确;B、若只有一种氧化产物,说明铁过量,铜没有参与反应,反应后溶质为硝酸亚铁,但是amol铁不一定完全反应,无法确定a与c的关系,B错误;C、若只有二种氧化产物,氧化产物可能为硝酸亚铁和硝酸铜或硝酸铜和硝酸铁,硝酸可能过量,稀硝酸不一定完全反应,则无法计算被还原的硝酸的量,C错误;D、若有三种氧化产物,氧化产物为硝酸铜、硝酸铁和硝酸亚铁,说明硝酸完全反应,根据反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O、Fe+4HNO3=Fe(NO3)3+NO↑+2H2O可知,被还原的硝酸的物质的量为cmol×1/4=0.25cmol,D正确;答案选BC。