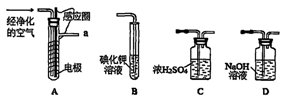
题目内容
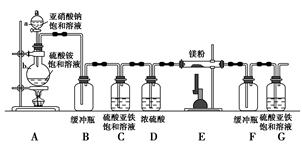
钙在加热时能与氮气、氢气反应。氢化钙遇水立即反应生成氢氧化钙和氢气,氢化钙通常用氢气与金属钙加热制取,图1是横拟制取装置。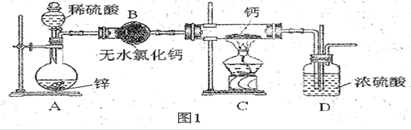
(1)用浓硫酸配制l:4(体积比)的稀硫酸,需用的玻璃仪器是烧杯、________。
(2)装置D中竖直导管的作用是________________________。
(3)为了确认进入装置C的氢气已经干燥,可在B、C之间再接一装置,该装置中加入的试剂是_______。加热C装置前要对H2验纯,方法是:收集一试管气体,将管口靠近酒精灯火焰,若听到“噗噗”的声音,说明H2__________________________。
(4)甲同学认为只要装置合理、操作规范就可以排除生成__________(选填序号)。
a.Ca3N2 b.CaO c.Ca(OH)2
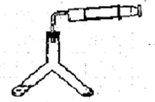
(5)乙同学用上图装置测定制得的氢化钙的纯度。他称取46 mg样品,与足量水反应,恒温时,注射器量出产生的气体为48.06 mL(已换算为标准状况)。产生实验误差的原因可能是_______(选填编号)。
①H2通入不足,反应器中有空气
②钙与H2未充分反应
③产物与空气接触
(6)丙同学根据乙同学的实验数据列了一个关系式,42x+40y=0.046、2x+y=48.06/22400请指出式子中y的含义___________________________________。
(1)玻璃棒、量筒(2分)
(2)平衡压强,防止液体倒流 (2分)
(3)无水硫酸铜(或其他合理答案)(1分);纯净(1分)
(4)a.b.c.(2分,答对2个就可以)
(5)①②(2分)
(6)钙的物质的量(2分)
解析试题分析:(1)用浓硫酸配制l:4(体积比)的稀硫酸,需用的玻璃仪器是烧杯、玻璃棒、量筒。
(2)装置D中竖直导管的作用是平衡压强,防止液体倒流 。
(3)为了确认进入装置C的氢气已经干燥,可在B、C之间再接一装置,该装置中加入的试剂是无水硫酸铜,通过观察是否变成蓝色进行判断。加热C装置前要对H2验纯,方法是:收集一试管气体,将管口靠近酒精灯火焰,若听到“噗噗”的声音,说明H2纯净。
(4)钙能和空气中的氮气,氧气及水都可能会反应,分别生成 a.Ca3N2 b.CaOc.Ca(OH)2,故选abc。
(5)根据CaH2 + 2H2O = Ca(OH)2 + 2H2 。48.06 mL(已换算为标准状况)物质的量是0.002mol。CaH2的质量为0.084g,即84mg。结果偏大。①H2通入不足,反应器中有空气,可能会生成Ca3N2和CaO,Ca3N2 --- 2NH3,可能会使气体的量增大,结果偏大。②钙与H2未充分反应,必将会发生Ca---H2 ,也会使气体的量增大,结果偏大。③产物与空气接触后有部分气体放出,结果会偏小,错误;
(6)根据42,这是氢化钙的相对分子质量,40是钙的相对原子质量,可知42x+40y=0.046、2x+y=48.06/22400请指出式子中y的含义钙的物质的量。
考点:本题考查硫酸的稀释,物质的制备及原理分析,实验误差分析和计算。

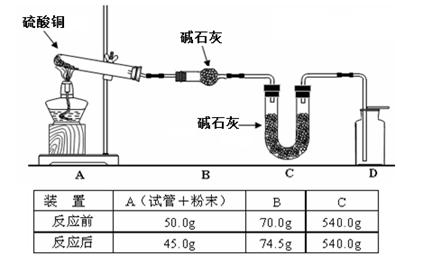
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。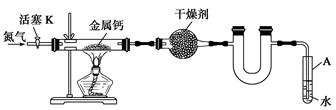
(1)反应过程中末端导管必须始终插入试管A的水中,目的是_____________________。
(2)制备氮化钙的操作步骤是:
①打开活塞K并通入N2;
②点燃酒精灯,进行反应;
③反应结束后,__________________________________________________________;
④拆除装置,取出产物。
(3)数据记录如下:(假设反应完全)
| 空硬质管质 量m0/g | 硬质管与钙的 质量m1/g | 硬质管与产物 的质量m2/g |
| 14.80 | 15.08 | 15.15 |
① 计算得到实验式CaxN2,其中x=________。
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:
______________________________________________________________________。
采用下列装置和操作,能达到实验目的的是
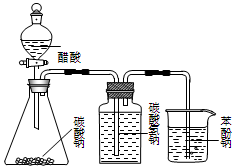


甲 乙 丙 丁
| A.甲装置:加热浓硫酸和乙醇(其体积为比3∶1)混合液,制取乙烯 |
| B.乙装置:比较醋酸、碳酸、苯酚三者的酸性强弱 |
| C.丙装置:向混有苯酚的苯中加入NaOH溶液,除去其中的苯酚 |
| D.丁装置:A中为乙醇、醋酸,B为饱和碳酸钠溶液,制取乙酸乙酯 |
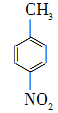 +Na2Cr2O7+4H2SO4―→
+Na2Cr2O7+4H2SO4―→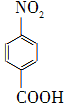 +Na2SO4+Cr2(SO4)3+5H2O
+Na2SO4+Cr2(SO4)3+5H2O

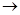

 +CaS+BaCl2。以下是从焙烧后的固体中分离得到氯化钡晶体的实验流程设计(已知硫化钙不溶于水,易溶于盐酸)。请在空格方框横线上填写操作名称。
+CaS+BaCl2。以下是从焙烧后的固体中分离得到氯化钡晶体的实验流程设计(已知硫化钙不溶于水,易溶于盐酸)。请在空格方框横线上填写操作名称。

 2O3)。
2O3)。