题目内容
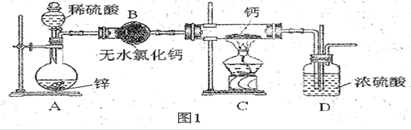
制备氮化镁的装置示意图如下: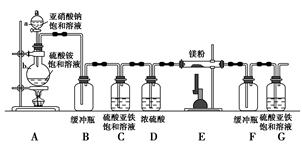
回答下列问题:
(1)检查装置气密性的方法是________________________________,
a的名称是________,b的名称是________;
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式___________________;
(3)C的作用是______________________________________________________,
D的作用是____________________________________________________,
是否可以把C和D的位置对调并说明理由_____________________________;
(4)写出E中发生反应的化学方程式_________________________________;
(5)请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出实验操作及现象____________________________________________________。
(1)微热b,这时G中有气泡冒出,停止加热冷却后,G中插在溶液里的玻璃管形成一段水柱,则气密性良好 分液漏斗 圆底烧瓶
(2)2NaNO2+(NH4)2SO4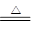 2N2↑+Na2SO4+4H2O
2N2↑+Na2SO4+4H2O
(3)除去氧气及氮氧化物 除去水蒸气 不能,对调后无法除去水蒸气
(4)N2+3Mg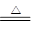 Mg3N2
Mg3N2
(5)取少量产物于试管中,加入少量蒸馏水,试管底部有沉淀生成,可闻到刺激性氨味(把湿润的红色石蕊试纸放在管口,试纸变蓝),证明产物中含有氮化镁;弃去上层清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁
解析

(11分)苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
已知:苯甲酸相对分子质量是122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在答题卡上完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热,溶解,Ⅰ | 得到白色晶体和无色溶液 | ———— |
| ② | 取少量滤液于试管中, Ⅱ | 生成白色沉淀 | 滤液含有Cl- |
| ③ | 干燥白色晶体, Ⅲ | Ⅳ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol。产品中苯甲酸质量分数为 (保留两位有效数字)。
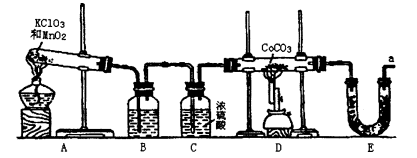
(18分)某化学兴趣小组的同学利用下图所示实验装置进行实验。(图中a、b、c表示止水夹)。

请按要求填空:
(1)利用B装置可制取的气体有 (至少填2种),写出实验室里利用A装置制取氯气的离子方程式 。
(2)只用A、C、E相连后的装置用于制取Cl2并进行相关的性质实验。若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
| 实验序号 | 实验操作 | 现 象 | 结 论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入 NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
①请评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由。 (任选1个实验进行评价。)
| 实验序号 | 结论 | 理由 |
| Ⅰ | | |
| Ⅱ | | |
②若要利用上述A、C装置设计一个简单的实验,验证Cl2和I2的氧化性强弱,可以在甲、乙、丙中分别装入浓盐酸、MnO2、淀粉碘化钾溶液,根据丙中产生的现象是 ,则可证明Cl2的氧化性强于I2 。
(3)B、D、E装置相连后,在B中盛装足量浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验。
①B中发生反应的化学方程式 。
② 欲用D装置验证NO2与水的反应,其操作步骤:先关闭止水夹 (填写a、b或c),再打开止水夹 (填写a、b或c),若要使D烧杯中的水进入试管丁的操作是:通过 试管丁,使试管丁的NO2气体逸出,NO2与水接触后即可引发烧杯中的水倒流进入试管丁。