题目内容
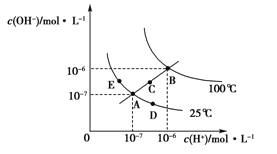
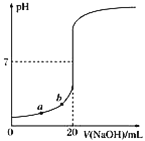
【题目】如图是用0.1000mol·L-1的NaOH溶液滴定20.00mL未知浓度盐酸(酚酞作指示剂)的滴定曲线,下列说法正确的是( )
A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.0100mol·L-1
C.指示剂变色时,说明盐酸与NaOH一定恰好完全反应
D.当滴加NaOH溶液10.00mL时,该混合液的pH=1+lg3
【答案】D
【解析】
A.随着NaOH溶液的不断加入,溶液中盐酸的浓度不断减小,所以a点盐酸的浓度大于b点,对水电离的抑制作用减弱,水电离出的氢离子浓度:a<b,A不正确;
B.V(NaOH)=20.00mL时,pH=7,盐酸的物质的量浓度为![]() 0.100mol·L-1,B不正确;
0.100mol·L-1,B不正确;
C.酚酞变色时,溶液的pH≥8.2,说明NaOH中和盐酸后,有少量剩余,C不正确;
D.当滴加NaOH溶液10.00mL时,该混合液的c(H+)=![]() =
=![]() mol/L,pH=-lgc(H+)=1+lg3,D正确;
mol/L,pH=-lgc(H+)=1+lg3,D正确;
故选D。

练习册系列答案
相关题目