题目内容
11.某同学用图中四种装置从海带里提取取碘,其中正确且能达到实验目的是( )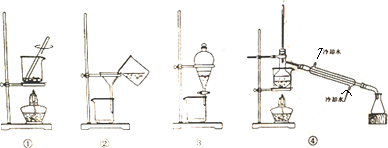
| A. | 装置①将海带灼烧成灰 | B. | 装置②过滤含I-的溶液 | ||
| C. | 装置③放出碘的CCl4溶液 | D. | 装置④分离碘并回收CCl4 |
分析 A.灼烧固体,应在坩埚中进行;
B.过滤时应用玻璃棒引流;
C.碘易溶于四氯化碳;
D.回收萃取剂苯并获得单质碘,可用蒸馏的方法,注意温度计的位置以及水的进出方向.
解答 解:A.灼烧固体温度较高,应在坩埚中进行,故A错误;
B.过滤时应用玻璃棒引流,故B错误;
C.碘易溶于四氯化碳,不能用分液的方法分离,应用蒸馏的方法,故C错误;
D.回收萃取剂苯并获得单质碘,可用蒸馏的方法,温度计位于蒸馏烧瓶的支管口,且水从下端进,上端出,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯及实验基本操作等为解答的关键,侧重提纯碘的实验及分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
6. 化学反应的快慢和限度对人类生产生活有重要的意义.
化学反应的快慢和限度对人类生产生活有重要的意义.
(1)将反应速率的影响条件填在空格处.
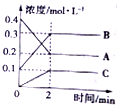
(2)800℃时,A、B、C三种气体在固定体积的密闭容器中反应,反应过程中各物质的浓度变化如图所示,分析图象回答问题:
①该反应的化学方程式为2A?2B+C;
(2)2min内,用C表示的反应速率为0.05mol/(L•min).
③在其他条件下,测得A的反应速率为0.05mol•L-1•min-1,此时的反应与800b℃时相比.
a.比800℃时快 b.比800℃时慢 c.与800℃时速率相等 d.无法确定
(3)判断该反应达到平衡状态的标志是ce
a.A和B的浓度相等
b.v(B)=2v(C)
c.容器内气体压强不再改变
d.密闭容器中混合气体的密度不变
e.容器内A的体积分数不再改变.
 化学反应的快慢和限度对人类生产生活有重要的意义.
化学反应的快慢和限度对人类生产生活有重要的意义.(1)将反应速率的影响条件填在空格处.
| 实例 | 影响条件 |
| ①食物放在冰箱里能延长保质期 | |
| ②工业炼铁时,把铁矿石预先粉碎后,再进行炼制 | |
| ③用H2O2分解制O2,加入MnO2 |
①该反应的化学方程式为2A?2B+C;
(2)2min内,用C表示的反应速率为0.05mol/(L•min).
③在其他条件下,测得A的反应速率为0.05mol•L-1•min-1,此时的反应与800b℃时相比.
a.比800℃时快 b.比800℃时慢 c.与800℃时速率相等 d.无法确定
(3)判断该反应达到平衡状态的标志是ce
a.A和B的浓度相等
b.v(B)=2v(C)
c.容器内气体压强不再改变
d.密闭容器中混合气体的密度不变
e.容器内A的体积分数不再改变.
16.下列热化学方程式中△H代表燃烧热的是( )
| A. | CH4 ( g )+$\frac{3}{2}$O2( g )═2H2O ( l )+CO ( g )△H1 | |
| B. | S ( s )+$\frac{3}{2}$O2 ( g )═SO3 ( s )△H2 | |
| C. | C6H12O6 ( s )+6O2 ( g )═6CO2 (g)+6H2O ( l )△H3 | |
| D. | 2CO ( g )+O2( g )═2CO2 ( g )△H4 |
3.在如右图所示的原电池中,下列说法正确的是( )
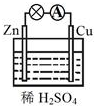

| A. | Zn为负极,Cu为正极 | B. | 正极反应式为:Zn-2e-═Zn2+ | ||
| C. | 负极反应式为:Cu-2e-═Cu2+ | D. | 该装置能将电能转化为化学能 |
1.2001年11月,美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了BLU-82高能燃料空气炸弹,该炸弹的成分之一是环氧乙烷,其化学式为C2H4O.下列有关说法中正确的是( )
| A. | 环氧乙烷是甲醛的同系物 | |
| B. | 环氧乙烷是乙醛的同分异构体,肯定能发生银镜反应 | |
| C. | 等质量的环氧乙烷与乙酸乙酯分别完全燃烧时耗氧量相同 | |
| D. | 环氧乙烷性质非常稳定,不易燃烧 |
 化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.
化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.