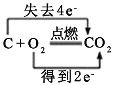
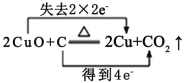
��Ŀ����
����Ŀ�����ͻ���β����![]() ����ȫ��Χ���ܹ�ע���ȵ����⡣
����ȫ��Χ���ܹ�ע���ȵ����⡣
(1)���ͻ���β���е�![]() �ǿ����е�
�ǿ����е�![]() �ڸ�����ȼ�����ɵģ������ɵķ�Ӧ�������£�
�ڸ�����ȼ�����ɵģ������ɵķ�Ӧ�������£�
A22A��
A+B2NO+B��
B��+A2NO+A��
��֪![]() ʱ�ļ������ݣ�
ʱ�ļ������ݣ�
��ѧ�� | O=O | N��N | N=O |
����/kJ��mol-1 | 498.0 | 946.0 | 630.0 |
������������![]() ��������________(����
��������________(����![]() ������
������![]() ��)���������жϵ�ԭ����________��
��)���������жϵ�ԭ����________��
�ڸ�������![]() �����ɻ�������д��ͨ��״����
�����ɻ�������д��ͨ��״����![]() ȼ������
ȼ������![]() ���Ȼ�ѧ����ʽ��________��
���Ȼ�ѧ����ʽ��________��
(2)TWC����������ȼ�ϲ���ȫȼ�����ɵ�![]() ��β���е�
��β���е�![]() ��ԭΪ������ļ������� 2NO+2CO
��ԭΪ������ļ������� 2NO+2CO![]() 2CO2+N2 ��H��0���ֽ���COa%(�����������ͬ)��NO0.30%��ģ������β����100mL��min-1������ͨ��450��ķ�Ӧ��������������CO�ĺ�����Ϊb%(��������仯���Բ���)����v(CO)=________mL��min-1��������Ӧ���¶Ƚ�����350�棬����������CO�ĺ���________b%(������������������=��)
2CO2+N2 ��H��0���ֽ���COa%(�����������ͬ)��NO0.30%��ģ������β����100mL��min-1������ͨ��450��ķ�Ӧ��������������CO�ĺ�����Ϊb%(��������仯���Բ���)����v(CO)=________mL��min-1��������Ӧ���¶Ƚ�����350�棬����������CO�ĺ���________b%(������������������=��)
(3)SCR����������![]() ��β���е�
��β���е�![]() ѡ���Ի�ԭΪ������ļ���������
ѡ���Ի�ԭΪ������ļ���������![]() ��ͨ������[CO(NH2)2]�ֽ����ɵģ�
��ͨ������[CO(NH2)2]�ֽ����ɵģ�
��.CO(NH2)2(s)NH3(g)+HNCO(g) H1
��.HNCO(g)+H2O(g)NH3(g)+CO2(g) H2
��һ���¶��£���һ�����ܱ�������Ͷ��������CO(NH2)2�����һ������ˮ����������������Ӧ������Ӧ�ﵽƽ��ʱ�����c(NH3)=pmol/L��c(HNCO)=qmol/L����Ӧ���ƽ�ⳣ��Ϊ________(�ú�p��q�ı���ʽ��ʾ����ͬ)��c(CO2)=________mol/L��
���ҹ���ѧ�����о��¶ȡ�����Ũ�ȶ�����ˮ�����Ũ�ȵ�Ӱ��õ��������ݣ�
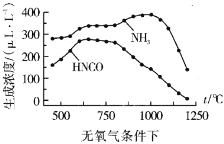
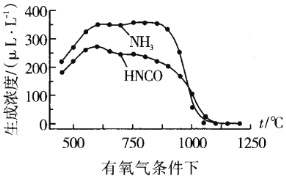
ͨ�����ݶԱȿ��Է�������������1100������ʱ����ϵ��![]() Ũ�Ƚӽ�0��LL-1�������ԭ��__
Ũ�Ƚӽ�0��LL-1�������ԭ��__
���𰸡�O2 O2��O=O���ܱ�N2��N��N����С��������Ϊԭ�� N2(g)+O2(g)=2NO(g) H=+184.0kJ/mol (a-b) �� qp ![]() �����ڸ���ʱ��NH3����
�����ڸ���ʱ��NH3����
��������
(1)��H=��Ӧ��ļ��ܺ�-������ļ��ܺͣ�
(2) ���v(CO)�ĵ�λmL��min-1���¶ȶ�ƽ����ƶ��������ɣ�
(3)���ݷ�Ӧԭ�������ƽ�ⳣ���ļ��㹫ʽ�Ͱ����Ļ�ԭ�Է�����
(1) ����֪O=O�ļ���Ϊ498.0 kJ��mol-1��N��N�ļ���Ϊ946.0 kJ��mol-1����O2��O=O���ܱ�N2��N��N����С��������Ϊԭ�ӣ�������������A2��������O2��
����֪N2(g)+O2(g)=2NO(g)������H=��Ӧ��ļ��ܺ�-������ļ��ܺ�=(946.0 kJ��mol-1)+(498.0 kJ��mol-1)-2(630.0 kJ��mol-1)=+184.0kJ/mol����ͨ��״����![]() ȼ������
ȼ������![]() ���Ȼ�ѧ����ʽΪN2(g)+O2(g)=2NO(g) H=+184.0kJ/mol��
���Ȼ�ѧ����ʽΪN2(g)+O2(g)=2NO(g) H=+184.0kJ/mol��
(2)��ͨ��ʱ��Ϊ1min����ÿͨ��100mL��������к�CO�����ΪamL������100mL��������к�CO�����ΪbmL����v(CO)=![]() =(a-b)mL��min-1����֪2NO+2CO
=(a-b)mL��min-1����֪2NO+2CO![]() 2CO2+N2 ��H��0����Ӧ���¶Ƚ�����350�棬ƽ�⽫�����ƶ���CO��ת������ߣ����³���������CO�ĺ�����b%��
2CO2+N2 ��H��0����Ӧ���¶Ƚ�����350�棬ƽ�⽫�����ƶ���CO��ת������ߣ����³���������CO�ĺ�����b%��
(3) �ٵ���Ӧ�ﵽƽ��ʱ�����c(NH3)=pmol/L��c(HNCO)=qmol/L����Ӧ���ƽ�ⳣ��K=c(NH3)��c(HNCO)= pq(mol/L)2��
��c(CO2)=cmol/L����HNCO(g)+H2O(g)NH3(g)+CO2(g)��֪��Ӧ�вμӷ�Ӧ��c(HNCO)������c(NH3)��Ϊcmol/L���ٸ���CO(NH2)2(s)NH3(g)+HNCO(g)��֪��Ӧ������c(HNCO)=c(NH3)����qmol/L- cmol/L= pmol/L+ cmol/L����ã�c=![]() ����c(CO2)=
����c(CO2)=![]() _mol/L��
_mol/L��
��ͨ���Ƚ��¶ȡ�����Ũ�ȶ�����ˮ�����Ũ�ȵ�Ӱ���������������1100������ʱ����ϵ��![]() Ũ�Ƚӽ�0��LL-1�������ԭ���ǰ����л�ԭ�ԣ��ڸ������ܱ�����������
Ũ�Ƚӽ�0��LL-1�������ԭ���ǰ����л�ԭ�ԣ��ڸ������ܱ�����������

 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�