题目内容
15.(1)下列变化(填序号)①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氧气溶于水⑥氯化铵受热分解.未发生化学键破坏的是①⑤;仅发生离子键破坏的是②③;仅发生共价键破坏的是④;既发生离子键又发生共价键破坏的是⑥;(2)用电子式写出MgCl2、HCl的形成过程
①MgCl2的形成过程:
 ;
;②HCl的形成过程:
 .
.
分析 (1)根据物质所含化学键的类型以及发生的变化是物理变化还是化学变化来分析;
(2)①MgCl2为离子化合物,根据离子化合物的电子式表示方法写出MgCl2的形成过程;
②HCl为共价化合物,根据共价化合物的电子式表示方法写出HCl的形成过程;
解答 解:(1)①碘的升华属于物理变化,只是状态发生变化,没有化学键的破坏;
②烧碱熔化中存在离子键,融化烧碱时,阴阳离子间的化学键被破坏,所以破坏的是离子键;
③氯化钠溶于水,在水分子的作用下,氯化钠中的离子键被破坏,所以破坏的是离子键;
④氯化氢溶于水,在水分子的作用下,氯化氢中的共价键被破坏,所以破坏的是共价键;
⑤氧气溶于水,属于物理变化,没有化学键的破坏;
⑥氯化铵受热分解,氯化铵是离子化合物,存在的化学键有离子键、共价键,受热分解时,阴阳离子间的化学键、及铵根离子中的共价键被破坏,所以所以破坏的是离子键、共价键;
故答案为:①⑤;②③;④;⑥.
(2)①MgCl2为离子化合物,用电子式表示MgCl2的形成过程为: ;
;
故答案为: ;
;
②HCl为共价化合物,用电子式表示HCl的形成过程为: ;
;
故答案为: ;
;
点评 本题考查了离子键、共价键的区别以及用电子式正确表示化合物的形成过程.侧重考查学生对概念的辨别能力,离子化合物中可能含有共价键,共价化合物中一定不含离子键.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
19.下列说法不正确的是( )
| A. | 激素类药物乙烯雌酚的结构简式为: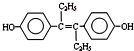 ,它的分子式是:C18H20O2 ,它的分子式是:C18H20O2 | |
| B. | 等质量的甲烷、乙烯、乙醇分别充分燃烧,所耗用氧气的量依次减少 | |
| C. | 聚乳酸(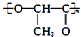 )是由单体之间通过加聚反应合成的 )是由单体之间通过加聚反应合成的 | |
| D. | 实验证实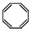 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键. 可使溴的四氯化碳溶液褪色,说明该分子中存在碳碳双键. |
20.根据表中给出的几种物质的熔沸点数据,判断下列说法错误的是( )
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质硼 | |
| 熔点/℃ | 810 | 710 | 180 | -68 | 2300 |
| 沸点/℃ | 1 465 | 1 418 | 160 | 57 | 2 500 |
| A. | SiCl4是分子晶体 | B. | 单质硼可能是原子晶体 | ||
| C. | AlCl3加热能升华 | D. | NaCl的键的强度比MgCl2的小 |
7.下列情况会对人体造成较大伤害的是( )
| A. | 用SO2漂白银耳 | |
| B. | 自来水中通入少量氯气消毒杀菌 | |
| C. | 用食醋清洗热水瓶胆内壁附着的水垢(水垢的主要成分为CaCO3、Mg(OH)2) | |
| D. | 用小苏打(NaHCO3)发酵面粉制作馒头 |
4.下列有关叙述中正确的是( )
| A. | 因为s轨道的形状是球形的,所以s电子做的是圆周运动 | |
| B. | 3px、3py、3pz的差异之处在于三者中电子(基态)的能量不同 | |
| C. | 原子轨道和电子云都是用来形象地描述电子运动状态的 | |
| D. | 电子云图上的每一个点都代表一个电子 |
5.关于锌、铜和稀硫酸构成的原电池的下列说法中正确的是( )
| A. | 锌是正极,铜是负极 | B. | 电子从铜片经导线流向锌片 | ||
| C. | 负极的反应式为2H++2e-=H2↑ | D. | 反应一段时间后,溶液的pH升高 |