题目内容
(12分)2008年9月25日我国“神七”成功发射,标志着我国载人航天技术迈出重要的一步。“神七”以N2H4和N2O4燃料,N2H4学名为肼又称联氨,无色油状液体,具有与氨相似的气味,毒性很大。
⑴水电离成H3O+和OH-叫做水的自偶电离。同水一样,N2H4也有微弱的自偶电离,其自偶电离的方程式为: 。
⑵氨显碱性的原因在于NH3分子中的N原子具有孤对电子,它能通过配位键结合水中的H+,使水电离出OH-,其过程可以表示为NH3+H2O NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。
NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。
⑶已知硼酸[B(OH)3]为一元弱酸,其显示酸性的原理与NH3、N2H4显示碱性的原理类似,试用离子方程式表示其显示酸性的过程: 。
⑷N2H4和N2O4反应温度达2700摄氏度,产生无污染的气体。1g液态N2H4与足量的液态N2O4充分反应生成两种气态物质,可放出a KJ热量,试写出该反应的热化学方程式:
。
⑴水电离成H3O+和OH-叫做水的自偶电离。同水一样,N2H4也有微弱的自偶电离,其自偶电离的方程式为: 。
⑵氨显碱性的原因在于NH3分子中的N原子具有孤对电子,它能通过配位键结合水中的H+,使水电离出OH-,其过程可以表示为NH3+H2O
 NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。
NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。⑶已知硼酸[B(OH)3]为一元弱酸,其显示酸性的原理与NH3、N2H4显示碱性的原理类似,试用离子方程式表示其显示酸性的过程: 。
⑷N2H4和N2O4反应温度达2700摄氏度,产生无污染的气体。1g液态N2H4与足量的液态N2O4充分反应生成两种气态物质,可放出a KJ热量,试写出该反应的热化学方程式:
。
⑴N2H4+N2H4 N2H5++N2H3-⑵ N2H4+2HCl=N2H6Cl2 ⑶B(OH)3+H2O
N2H5++N2H3-⑵ N2H4+2HCl=N2H6Cl2 ⑶B(OH)3+H2O [B(OH)4]-+H+ ⑷N2H4(l)+N2O4(l)=N2(g)+H2O(g);△H=-32a KJ/mol。(每空3分)
[B(OH)4]-+H+ ⑷N2H4(l)+N2O4(l)=N2(g)+H2O(g);△H=-32a KJ/mol。(每空3分)
 N2H5++N2H3-⑵ N2H4+2HCl=N2H6Cl2 ⑶B(OH)3+H2O
N2H5++N2H3-⑵ N2H4+2HCl=N2H6Cl2 ⑶B(OH)3+H2O [B(OH)4]-+H+ ⑷N2H4(l)+N2O4(l)=N2(g)+H2O(g);△H=-32a KJ/mol。(每空3分)
[B(OH)4]-+H+ ⑷N2H4(l)+N2O4(l)=N2(g)+H2O(g);△H=-32a KJ/mol。(每空3分) 根据水的自偶电离可知,自偶电离即两个相同分子之间转移带电的粒子, 可知N2H4应转移H+,其反应为N2H4+N2H4 N2H5++N2H3-。由于N2H4有两个孤对电子,能与2个H+结合,故1mol N2H4最多能与2molHCl反应。由NH3、N2H4显碱性是因为结合水中的H+,可以推知B(OH)3显酸性应结合水中的OH-,故B(OH)3表现酸性的过程为B(OH)3+H2O
N2H5++N2H3-。由于N2H4有两个孤对电子,能与2个H+结合,故1mol N2H4最多能与2molHCl反应。由NH3、N2H4显碱性是因为结合水中的H+,可以推知B(OH)3显酸性应结合水中的OH-,故B(OH)3表现酸性的过程为B(OH)3+H2O [B(OH)4]-+H+。由题中信息指出“N2H4和N2O4反应产生无污染的气体”可知N在产物中以N2形式存在,进而可知另一物质为H2O。
[B(OH)4]-+H+。由题中信息指出“N2H4和N2O4反应产生无污染的气体”可知N在产物中以N2形式存在,进而可知另一物质为H2O。
【技巧点拨】本题通过信息迁移考查学生自学能力和应用能力。对信息迁移的主要方式就是类比。在进行类比时,首先要弄清信息本质(即所体现的化学原理),并找出信息与问题的相似点,然后结合相似点再将信息说明的原理应用于问题之中,其中深入理解信息本质是解决问题的关键。比如N2H4有孤对电子与缺电子的H+结合是利用了⑵中体现的“配位原理”,其实缺电子的B(OH)3结合有孤对电子的OH-也是利用了就有了“配位原理”。由于问题⑶在问题⑵的基础上有了较大的提升,如果不明白其原理,则很难完成类比。
 N2H5++N2H3-。由于N2H4有两个孤对电子,能与2个H+结合,故1mol N2H4最多能与2molHCl反应。由NH3、N2H4显碱性是因为结合水中的H+,可以推知B(OH)3显酸性应结合水中的OH-,故B(OH)3表现酸性的过程为B(OH)3+H2O
N2H5++N2H3-。由于N2H4有两个孤对电子,能与2个H+结合,故1mol N2H4最多能与2molHCl反应。由NH3、N2H4显碱性是因为结合水中的H+,可以推知B(OH)3显酸性应结合水中的OH-,故B(OH)3表现酸性的过程为B(OH)3+H2O [B(OH)4]-+H+。由题中信息指出“N2H4和N2O4反应产生无污染的气体”可知N在产物中以N2形式存在,进而可知另一物质为H2O。
[B(OH)4]-+H+。由题中信息指出“N2H4和N2O4反应产生无污染的气体”可知N在产物中以N2形式存在,进而可知另一物质为H2O。【技巧点拨】本题通过信息迁移考查学生自学能力和应用能力。对信息迁移的主要方式就是类比。在进行类比时,首先要弄清信息本质(即所体现的化学原理),并找出信息与问题的相似点,然后结合相似点再将信息说明的原理应用于问题之中,其中深入理解信息本质是解决问题的关键。比如N2H4有孤对电子与缺电子的H+结合是利用了⑵中体现的“配位原理”,其实缺电子的B(OH)3结合有孤对电子的OH-也是利用了就有了“配位原理”。由于问题⑶在问题⑵的基础上有了较大的提升,如果不明白其原理,则很难完成类比。

练习册系列答案
相关题目
 请回答氯碱的如下问题:
请回答氯碱的如下问题: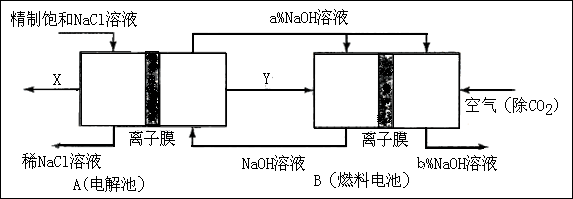 图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;