题目内容
【题目】钠与水反应的实验过程如图①、②、③所示,下列有关说法不正确的是
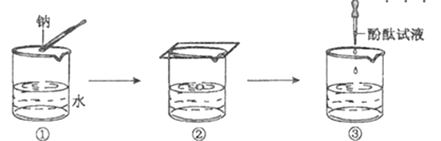
A. 图②中钠熔成小球,说明钠与水反应放热且钠的熔点低
B. 图②中钠四处游动并嘶嘶作响,说明反应产生了气体
C. 图③中滴加酚酞试液后溶液变红,说明有碱性物质生成
D. 钠与水反应的离子方程式是: 2Na+ 2H+=2Na+ + H2↑
【答案】D
【解析】
根据实验现象分析判断。
A项:图②中钠熔成小球所需热量必为反应放出,此时水未沸腾,则钠的熔点低于100℃,A项正确;
B项:图②中钠球游动是反应产生气体的推动,B项正确;
C项:图③中是碱性物质使酚酞变红,C项正确;
D项:水是氧化物、也是难电离物质,不能拆写,应写成 2Na+ 2H2O=2Na+ +2OH-+ H2↑,D项错误。
本题选D。

练习册系列答案
相关题目