题目内容
13.氧气、甲烷和氮气混合气密度与相同条件下一氧化碳密度相等,求三种气体的物质的量比.分析 氧气、甲烷和氮气混合气密度与相同条件下一氧化碳密度相等,则混合气体和一氧化碳的相对分子质量相等,其中氮气、一氧化碳的相对分子质量都为28,可知氧气、甲烷的平均相对分子质量为28,以此解答该题.
解答 解:氧气、甲烷和氮气混合气密度与相同条件下一氧化碳密度相等,则混合气体和一氧化碳的相对分子质量相等,其中氮气、一氧化碳的相对分子质量都为28,可知氧气、甲烷的平均相对分子质量为28,
设氧气为xmol,甲烷为ymol,则$\frac{32x+16y}{x+y}$=28,x:y=3:1,
则三种气体的物质的量比3:1:任意值,
答:三种气体的物质的量比3:1:任意值.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握密度与相对原子质量的关系,难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
3.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1盐酸的澄清透明溶液:Fe3+、K+、SO${\;}_{4}^{2-}$、Br- | |
| B. | 含有硝酸钠的溶液:H+、Fe2+、Cl-、SO${\;}_{4}^{2-}$ | |
| C. | 能使石蕊变红的溶液:Cu2+、Na+、AlO${\;}_{2}^{-}$、Cl- | |
| D. | 由水电离出的c(H+)•c(OH-)=10-22的溶液:Na+、Ca2+、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$ |
1.我国最早报道的超高温导体中,铊是重要组成之一.已知铊是ⅢA族元素,关于铊的性质判断正确的是( )
| A. | 铊既能与强酸反应又能与强碱反应 | B. | 能生成+3价的化合物 | ||
| C. | Tl(OH)3与Al(OH)3一样是两性氢氧化物 | D. | Tl(OH)3的碱性比Al(OH)3强 |
5.0.1mol KClO3和0.1mol KClO中所含微粒数相等的是( )
| A. | 钾离子 | B. | 氯离子 | C. | 氯原子 | D. | 氧原子 |
2.一定条件下,乙醛可发生分解:CH3CHO(1)→CH4+CO,已知该反应的活化能为190.在含有少量I2的溶液中,该反应的机理为:
反应Ⅰ:CH3CHO+I2→CH3I+HI+CO(慢)
反应Ⅱ:CH3I+HI→CH4+I2
下列有关该反应的叙述中正确的是( )
反应Ⅰ:CH3CHO+I2→CH3I+HI+CO(慢)
反应Ⅱ:CH3I+HI→CH4+I2
下列有关该反应的叙述中正确的是( )
| A. | 反应速率与I2的浓度有关 | |
| B. | HI在反应I中是氧化产物 | |
| C. | 反应焓变的绝对值等于190kJ•mol-1 | |
| D. | 乙醛的分解速率主要取决于反应Ⅱ |
3.设NA为阿伏伽德罗常数,下列说法错误的是( )
| A. | 1mol H2O所含电子数为10NA | |
| B. | 1mol Al与足量的稀盐酸溶液反应生成氢气1.5mol | |
| C. | 在标准状况下,0.5NA Cl2所占的体积约是11.2L | |
| D. | 在非标准状况下,22.4L O2含有的分子数一定不是NA |
 .(2)HClO:
.(2)HClO: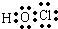 .
.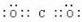 .(4)MgCl2:
.(4)MgCl2: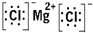 .
. . (6)H2S:
. (6)H2S: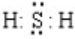 .
.