��Ŀ����
һ���¶��£���3 mol A�����1 mol B����ͨ��һ�ܱ������У��������·�Ӧ��3A(g)+B(g)  xC(g)������д���пհף�
xC(g)������д���пհף�
��1)����������̶�Ϊ2 L,��Ӧ2minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
��2min�ڣ�A��ƽ����Ӧ����Ϊ_______________��x= ��
��4min��C��Ũ��___________0.8 mol/L (����ڡ��������ڡ� ��С�ڡ�)��
����֪ƽ��������C���������Ϊ25������B��ת����________��
�ܸı���ʼ���ʼ����������ʹ��Ӧ�ﵽƽ��ʱC�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵ����ֱ�Ϊa��b��c������֮��Ӧ������Ĺ�ϵʽΪ________ ��
��
��2)��ά������ѹǿ���䣺
�ٴﵽƽ��ʱC���������__________25��(����ڡ��������ڡ���С�ڡ�)��
�ڸı���ʼ���ʼ����������ʹ��Ӧ�ﵽƽ��ʱC�����ʵ�����ԭƽ���2������Ӧ����_________mol A�����__________mol B���塣����Ҫ��д������̣�
��1���� 0.3 ��x= 2 ���� �� �� �� 40% ��
��
��2���� ���� �� �� 6 �� 2
����

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д���18�֣�A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������AԪ�صĵ�������Ȼ����������壬E�����뱣����ú���С�A��B��C�ֱɵ�������ȵĻ�����M��N����M��һ���ܲ�������ЧӦ������л��������ʣ�DԪ�������������Ǵ�����������3�����ش��������⣺
��1��N�ĵ���ʽΪ ��M�����к��� ������ԡ��Ǽ��ԡ�����
��2��D��E��1:1�γɵĻ�������ˮ��Ӧ�Ļ�ѧ��Ӧ����ʽ
(3)A��B��C��D���γ������Ӻ������Ӹ�������1��1�����ӻ�����X��A��D��E���γɻ�����Y��X��Y�����ʵ���֮��1��2���ȷ�Ӧ��д����Ӧ�Ļ�ѧ����ʽ
��Ӧ��ˮ��Һ�� ����ᡱ������С�����,ԭ���� �������ӷ���ʽ��ʾ��
��4����N��D�ĵ��ʡ�KOH��Һ����ԭ��أ����������C�ĵ��ʡ����为����ӦΪ ��һ��ʱ�����ҺpH ���������С�����䡱����
 ��5����һ���¶��£���4 mol C���ʺ�12 mol A����ͨ�뵽���Ϊ2L���ܱ������У�������Ӧ��2
min�ﵽƽ��״̬ʱ��A���ʵ�ת������50%������A���ʱ�ʾ�÷�Ӧ��ƽ������Ϊ
�����¶��µ�ƽ�ⳣ��ΪK=
��
��5����һ���¶��£���4 mol C���ʺ�12 mol A����ͨ�뵽���Ϊ2L���ܱ������У�������Ӧ��2
min�ﵽƽ��״̬ʱ��A���ʵ�ת������50%������A���ʱ�ʾ�÷�Ӧ��ƽ������Ϊ
�����¶��µ�ƽ�ⳣ��ΪK=
��
�ӻ�ѧƽ���ƶ��ĽǶȷ��������A���ʵ�ת���ʿ��Բ�ȡ�Ĵ�ʩ�� ��ѡ�������ĸ����
a����ʱ����������� b��ƽ����ټ���6molA���� c������ѹǿ d��ʹ�ô��� e��ƽ����ټ���2molC����
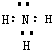
 HCO3-+OH-
HCO3-+OH-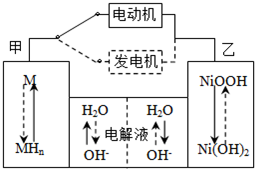
 n C��g��+q D��s����
n C��g��+q D��s����