题目内容
16.有NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应:①若所含溶质的物质的量相等,则生成沉淀的物质的量之比是1:2:3;②若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量之比是6:3:2.分析 ①若所含溶质的物质的量相等,假设NaCl、CaCl2、AlCl3均为1mol,根据氯离子守恒计算生成AgCl的物质的量之比;
②若生成沉淀AgCl的质量相等,设AgCl为1mol,根据氯离子守恒计算NaCl、CaCl2、AlCl3的物质的量.
解答 进而:①若所含溶质的物质的量相等,假设NaCl、CaCl2、AlCl3均为1mol,根据氯离子守恒,则生成AgCl分别为1mol、2mol、3mol,故生成AgCl的物质的量之比为1:2:3,故答案为:1:2:3;
②若生成沉淀AgCl的质量相等,设AgCl为1mol,根据氯离子守恒,则n(NaCl)=1mol、n(CaCl2)=0.5mol,n(AlCl3)=$\frac{1}{3}$mol,故NaCl、CaCl2、AlCl3的物质的量之比=1mol:0.5mol:$\frac{1}{3}$mol=6:3:2,故答案为:6:3:2.
点评 本题考查化学方程式计算,比较基础,注意利用赋值法与守恒法解答

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
7.将一小块金属钠投入下列水溶液中,有白色沉淀生成的是( )
| A. | Fe2(SO4)3 | B. | Ca(HCO3)2 | C. | NH4HCO3 | D. | 饱和澄清石灰水 |
4.下列说法正确的是( )
| A. | 质量相同、密度不同的CO与N2所含的原子数目一定相等 | |
| B. | 质量不同、密度相同的CO与N2所含分子数可能相同 | |
| C. | 分子数不同的CO与N2的体积一定不等 | |
| D. | 体积相同的CO与N2的质量一定相等 |
1.下列叙述正确的是( )
| A. | 64g SO2气体中含有6.02×1023个SO2分子 | |
| B. | 常温常压下,4.6g NO2气体含有3.01×1022个原子 | |
| C. | CuSO4•5H2O的摩尔质量为160g/mol | |
| D. | 标准状况下,33.6L CCl4含有9.03×1023个CCl4分子 |
5.下列实验操作正确的是( )
| A. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| B. | 配制一定物质的量浓度溶液时,在溶解、移液、洗涤、定容时均要用到玻璃棒 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |

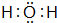 ,另一种能与E2-反应,该反应的离子方程式为4H2O2+S2-=SO42-+4H2O;
,另一种能与E2-反应,该反应的离子方程式为4H2O2+S2-=SO42-+4H2O;