题目内容
4.下列说法正确的是( )| A. | 质量相同、密度不同的CO与N2所含的原子数目一定相等 | |
| B. | 质量不同、密度相同的CO与N2所含分子数可能相同 | |
| C. | 分子数不同的CO与N2的体积一定不等 | |
| D. | 体积相同的CO与N2的质量一定相等 |
分析 A.根据n=$\frac{m}{M}$判断CO与N2物质的量关系,CO与N2分子均含有2个原子,若二者物质的量相等,则含有原子数目相等;
B.根据n=$\frac{m}{M}$判断CO与N2物质的量关系,分子数目之比等于物质的量之比;
C.分子数目不同,则物质的量不同,根据PV=nRT可知,它们的体积可能相同;
D.CO与N2的摩尔质量相等,体积相同的CO与N2,由于温度、压强会影响物质的量,二者物质的量不一定相等.
解答 解:A.CO与N2的摩尔质量相等,根据n=$\frac{m}{M}$可知,质量相同的CO与N2的物质的量相等,CO与N2分子均含有2个原子,则二者含有原子数目相等,故A正确;
B.CO与N2的摩尔质量相等,根据n=$\frac{m}{M}$可知,质量不同的CO与N2的物质的量不相等,则二者含有分子数目不相等,故B错误;
C.分子数目不同,则物质的量不同,根据PV=nRT可知,它们的体积可能相同,故C错误;
D.体积相同的CO与N2,由于温度、压强会影响气体物质的量,二者物质的量不一定相等,CO与N2的摩尔质量相等,则二者质量不一定相等,故D错误,
故选:A.
点评 本题考查阿伏伽德罗定律及其推论,难度不大,注意对公式的理解与灵活应用,注意根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列化学用语表达正确的是( )
| A. | 乙烯分子的比例模型: | B. | 硝基苯的结构简式: | ||
| C. | 羟基的电子式: | D. | 乙炔的结构简式:CHCH |
15.若将6C原子的核外电子排布式写成1s22s22p${\;}_{x}^{2}$,它违背了( )
| A. | 能量守恒原理 | B. | 能量最低原则 | C. | 泡利不相容原理 | D. | 洪特规则 |
12.现有两正盐的稀溶液,分别是a mol•L-1NaX溶液和b mol•L-1NaY溶液.下列说法不正确的是( )
| A. | 若a>b,测得c(X-)=c(Y-),可推出溶液中的c(HX)>c(HY) | |
| B. | 若a>b,测得c(X-)=c(Y-),可推出溶液中的c(HX)=c(HY) | |
| C. | 若a=b,且pH(NaX)>pH(NaY),则相同浓度时,酸性HX<HY | |
| D. | 若a=b,并测得a=c(X-)=c(Y-)+c(HY),则HX是强酸,HY是弱酸 |
19.化合物Y2X在水中能电离出具有相同电子层结构的阴阳离子,该化合物可能为( )
| A. | H2O | B. | Na2O | C. | KCl | D. | Na2S |
9.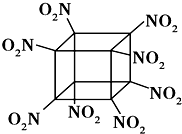 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )| A. | 分子中C、N间形成非极性键 | |
| B. | 1mol该分子中含8mol二氧化氮 | |
| C. | 该物质可能由立方烷发生取代反应而得 | |
| D. | 该物质爆炸产物是NO2、C02、H20 |