题目内容
【题目】【2016届临沂一模】二氧化氯(ClO2)是一种黄绿色易溶于水的气体,常用作饮用水消毒。实验室通过如下过程制备二氧化氯。
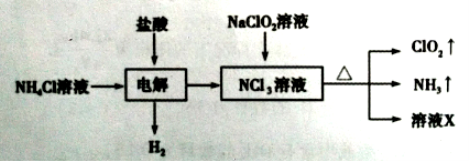
下列说法正确的是
A.电解时发生反应的离子方程式为NH4++3Cl-![]() 2H2↑+NCl3
2H2↑+NCl3
B.溶液X中大量存在的阴离子有Cl-、OH-
C.可用饱和食盐水除去ClO2中的NH3
D.可用明矾除去饮用水中残留的NaClO2
【答案】B
【解析】
试题分析:A、电解氯化铵与盐酸混合溶液,生成NCl3与H2,离子方程式为NH4++2H++3Cl-![]() 3H2↑+NCl3,A错误;B、根据元素守恒,溶液X中大量存在的阴离子有Cl-、OH-,B正确;C、ClO2 易溶于水,NH3 显碱性,因此要除去混有的氨气,应该选择浓硫酸,C错误;D、明矾在水中会生成氢氧化铝胶体,吸附水中的杂质起到净水的作用,但并不能除去NaClO2,D错误。答案选B。
3H2↑+NCl3,A错误;B、根据元素守恒,溶液X中大量存在的阴离子有Cl-、OH-,B正确;C、ClO2 易溶于水,NH3 显碱性,因此要除去混有的氨气,应该选择浓硫酸,C错误;D、明矾在水中会生成氢氧化铝胶体,吸附水中的杂质起到净水的作用,但并不能除去NaClO2,D错误。答案选B。

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
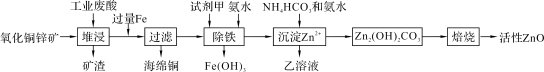
【题目】某科研小组设计出利用工业废酸(含10%的H2SO4)和废弃氧化铜锌矿制取活性ZnO的方案如图。
已知:298 K时各离子开始沉淀及完全沉淀时的pH如下表所示。
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 6.34 | 9.7 |
Fe3+ | 1.48 | 3.2 |
Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)____Ksp(ZnS)(选填“>”、“<”或“=”)。
(2)除铁过程中试剂甲最好选用____(填序号)。
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在____范围之间。
(4)试写出沉淀Zn2+时发生反应的离子方程式:____。