题目内容
9.用一种NaOH试剂,可将Na2SO4、MgSO4和Al3(SO4)2三种无色溶液区分开来.分析 这几种物质的阴离子相同、阳离子不同,Na+和NaOH不反应、Mg2+和NaOH反应生成白色沉淀、Al3+和过量NaOH反应先生成沉淀后沉淀溶解,可以用NaOH溶液鉴别这几种物质.
解答 解:这几种物质的阴离子相同、阳离子不同,Na+和NaOH不反应、Mg2+和NaOH反应生成白色沉淀、Al3+和过量NaOH反应先生成沉淀后沉淀溶解,离子反应方程式为Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O,现象不同,所以可以用NaOH溶液鉴别这几种物质,
故答案为:NaOH.
点评 本题考查物质鉴别实验方案设计,明确物质性质差异性是解本题关键,根据和同一物质反应不同现象来鉴别,难点是试剂的正确选取,题目难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
20.CO与H2在催化剂作用下合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g).在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温.实验测得相关数据如图1和图2.
下列有关说法正确的是( )
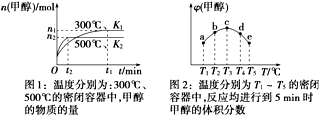
下列有关说法正确的是( )

| A. | 该反应的正反应是气体体积减小的吸热反应 | |
| B. | K1<K2(K为该条件下反应的平衡常数) | |
| C. | 反应进行到5 min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动 | |
| D. | 将容器c中的平衡状态时的甲醇体积分数转变到容器d中的平衡状态的甲醇体积分数,可采取的措施有升温或减压 |
17.反应A+3B2?2C+2D在四种不同情况下的反应速率分别为( )
①v(A)=0.15mol•L-1•s-1②v(B)=0.6mol•L-1•s-1
③v(C)=0.4mol•L-1•s-1 ④v(D)=0.45mol•L-1•s-1
该反应进行的快慢顺序为:
①v(A)=0.15mol•L-1•s-1②v(B)=0.6mol•L-1•s-1
③v(C)=0.4mol•L-1•s-1 ④v(D)=0.45mol•L-1•s-1
该反应进行的快慢顺序为:
| A. | ②>④>③>① | B. | ④>③>②>① | C. | ④>③=②>① | D. | ②>③=④>① |
4.下列实验能获得成功的是( )
| A. | 用纯碱溶液可鉴别出CCl4、C6H6、C2H5OH、CH3COOH | |
| B. | 用溴水、苯、铁屑制取溴苯 | |
| C. | 将无水乙醇加热到170℃制取乙烯 | |
| D. | 将冰醋酸、乙醇和2mol/L的硫酸加热制取乙酸乙酯 |
14.某HCl溶液的pH=1.0,则该盐酸溶液中c(H+)为( )mol/L.
| A. | 0.1 | B. | 1×10-3 | C. | 1×10-7 | D. | 1×10-13 |
1.下列说法正确的是( )
| A. | 蛋白质、纤维、蔗糖、聚乙烯、淀粉都是高分子化合物 | |
| B. | 研制乙醇汽油(汽油中添加一定比例的乙醇)技术,可以降低机动车辆尾气中有害气体排放 | |
| C. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| D. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
18.在硫酸铝、硫酸钾和明矾[KAl(SO4)2•12H2O]的混合溶液中,SO42-的浓度为4mol/L,当加入等体积4mol/L KOH溶液时,生成的沉淀恰好完全溶解,则反应后溶液中K+的浓度约为( )
| A. | 9 mol/L | B. | 4.5 mol/L | C. | 2.5 mol/L | D. | 2.25 mol/L |
9.Ⅰ、下表所列物质(括号内为少量杂质),在B中选择试剂,在C中选择操作的方法.填表(填入序号):
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;(7)KMnO4溶液.
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气.
Ⅱ、1mol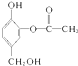 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;(7)KMnO4溶液.
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气.
| 物质 | 加入试剂 | 操作方法 |
| ①苯(苯甲酸) | (2) | (4) |
| ②乙酸乙酯(乙醇) | (5) | (4) |
 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.