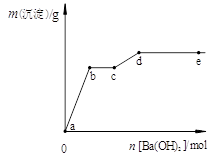
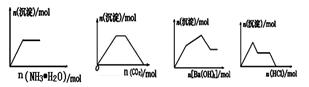
题目内容
下列说法正确的是
| A.浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂 |
B.在任何条件下都不能发生Cu+H2SO4=CuSO4+H2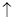 反应 反应 |
| C.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 |
| D.二氧化氮与水反应的离子方程式是3NO2+H2O=2HNO3+NO |
A
A、正确,HCL中+1价的氢化合价可以降低,具有氧化性,—1价的氯化合价处于最低价,可以升高,具有还原性,所以浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂;B、不正确,用铜作电极通过电解稀硫酸可以实现Cu+H2SO4 CuSO4+H2
CuSO4+H2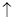 ;C、不正确,还原性I― >Fe2+ >Br― ,分别通入少量氯气,FeBr2中先发生Cl2+2Fe2+=2Fe3++2Cl―,不是置换反应。D、不正确,HNO3是强电解质,应拆开,3NO2+H2O=2H+ +NO3―+NO。选A。
;C、不正确,还原性I― >Fe2+ >Br― ,分别通入少量氯气,FeBr2中先发生Cl2+2Fe2+=2Fe3++2Cl―,不是置换反应。D、不正确,HNO3是强电解质,应拆开,3NO2+H2O=2H+ +NO3―+NO。选A。
 CuSO4+H2
CuSO4+H2 ;C、不正确,还原性I― >Fe2+ >Br― ,分别通入少量氯气,FeBr2中先发生Cl2+2Fe2+=2Fe3++2Cl―,不是置换反应。D、不正确,HNO3是强电解质,应拆开,3NO2+H2O=2H+ +NO3―+NO。选A。
;C、不正确,还原性I― >Fe2+ >Br― ,分别通入少量氯气,FeBr2中先发生Cl2+2Fe2+=2Fe3++2Cl―,不是置换反应。D、不正确,HNO3是强电解质,应拆开,3NO2+H2O=2H+ +NO3―+NO。选A。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目