题目内容
某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液体积变化的曲线如下图所示。据图判断下列叙述中,正确的是
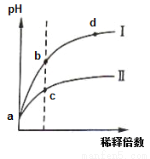
A.Ⅰ为氯化铵稀释时pH值变化曲线,Ⅱ为盐酸稀释时pH值变化曲线
B.b点溶液中水的电离程度比d点溶液中水的电离程度大,但两点的KW相同
C.a点时,等体积的两溶液分别与NaOH反应,消耗的NaOH量相同
D.c点溶液的导电能力一定比b点溶液导电能力强
D
【解析】
试题分析:A、盐酸为强酸,氢离子完全电离。氯化铵水解得到氢离子,加水稀释的同时水解程度增大,氢离子浓度减小的同时有所增加,所以变化较小,Ⅰ为盐酸稀释时pH值变化曲线,Ⅱ为氯化铵稀释时pH值变化曲线,故A错;B、b、d两点pH均小于7,b点溶液中氢离子浓度大,对水的电离抑制作用强,所以b点水的电离程度比d点溶液中水的电离程度小,错误;C、pH相同的盐酸和氯化铵,氯化铵浓度大,等体积的两溶液氯化铵消耗的氢氧化钠多,错误;D、C点离子浓度大,导电能力强,正确。
考点:考查盐类的水解、溶液稀释等知识。

练习册系列答案
相关题目