题目内容
下列说法错误的是( )
| A、浓硫酸具有强氧化性,但SO2气体可以用浓硫酸干燥 | B、常温下实验室可以用稀硝酸与铁反应制取NO气体 | C、从海水中提取溴的过程中常鼓入热空气,其目的是氧化Br- | D、SiO2不仅能与氢氧化钠溶液反应,也能与氢氟酸反应 |
分析:A.浓硫酸具有吸水性可做干燥剂,但是浓硫酸具有强氧化性和酸性,所以不能干燥还原性和碱性体贴;
B.常温下实验室可以用稀硝酸与铁或者铜反应制取NO气体;
C.海水中的溴元素以溴离子的形式存在,通入氯气将其氧化为溴单质,鼓入热空气,降低溴的溶解度,将溴吹出;
D.SiO2与氢氧化钠溶液反应生成硅酸钠和水,SiO2与氢氟酸生成四氟化硅和水.
B.常温下实验室可以用稀硝酸与铁或者铜反应制取NO气体;
C.海水中的溴元素以溴离子的形式存在,通入氯气将其氧化为溴单质,鼓入热空气,降低溴的溶解度,将溴吹出;
D.SiO2与氢氧化钠溶液反应生成硅酸钠和水,SiO2与氢氟酸生成四氟化硅和水.
解答:解:A.因为浓硫酸中的硫为+6价,二氧化硫中的硫为+4价,没有中间价态,二氧化硫虽然具有还原性,不能发生氧化还原反应,可以用浓硫酸干燥二氧化硫,故A正确;
B.常温下实验室可以用稀硝酸与铁或者铜反应制取NO气体,故B正确;
C.鼓入热空气的目的是降低溴的溶解度,将溴吹出,故C错误;
D.SiO2与氢氧化钠溶液反应:SiO2+2NaOH=Na2SiO3+H2O,二氧化硅与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O,故D正确;
故选C.
B.常温下实验室可以用稀硝酸与铁或者铜反应制取NO气体,故B正确;
C.鼓入热空气的目的是降低溴的溶解度,将溴吹出,故C错误;
D.SiO2与氢氧化钠溶液反应:SiO2+2NaOH=Na2SiO3+H2O,二氧化硅与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O,故D正确;
故选C.
点评:本题考查了浓硫酸的特性、海水提溴的流程、硝酸的性质、二氧化硅的性质,题目难度不大,只要记住相应物质的性质,不难找到答案.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法错误的是( )
| A、C2H4和C4H8一定都能使溴水退色 | B、C2H6和C4H10一定是同系物 | C、C3H6不只表示一种物质 | D、烯烃中各同系物中碳的质量分数相同 |
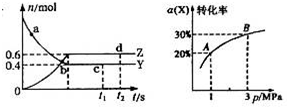 (2013?枣庄二模)一定温度下的密闭容器中发生反应:X(g)+3Y(g)f?2Z(g)△H<0,如图是反应达平衡及改变条件平衡移动的图象.下列说法错误的是( )
(2013?枣庄二模)一定温度下的密闭容器中发生反应:X(g)+3Y(g)f?2Z(g)△H<0,如图是反应达平衡及改变条件平衡移动的图象.下列说法错误的是( )