��Ŀ����
����Ŀ����������ʵ��������������õ��Ľ�����ȷ����
ѡ�� | ʵ��������� | ʵ����� |
A | ��ij��ɫ��Һ�м������KI��Һ,��Һ����ɫ | ��Һ�к���Br2 |
B | ��ij��Һ��ϡ���ᷴӦ����������ͨ�����ʯ��ˮ,ʯ��ˮ����� | ����Һ��һ������CO32- |
C | ����ʢ������NH4HCO3 ������Թ�,�����Թܿڷ���ʪ��ĺ�ɫʯ����ֽ,ʯ����ֽ���� | NH4HCO3�ʼ��� |
D | ����õ�Na2SO3 ��Һ�м�������BaCl2��Һ,���ְ�ɫ����,�ټ�������ϡ����,���������ܽ� | Na2SO3 ���ֱ����� |
A. AB. BC. CD. D
���𰸡�D
��������
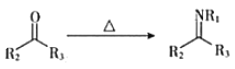
![]() Ҳ�ܰ�I-����Ϊ�ⵥ�ʣ�������Һ�п�����
Ҳ�ܰ�I-����Ϊ�ⵥ�ʣ�������Һ�п�����![]() ����A������
����A������![]() ��
��![]() ���������ᷴӦ�ų�������̼����B������̼�������Һ�ų�������������ʹʪ���ʯ����ֽ����������֤��̼��������Һ�ʼ��ԣ���C ��������õ�����������Һ�м����������Ȼ�����Һ�����ְ�ɫ�������ټ���ϡ���ᣬ���������ܽ⣬˵�������ᱵ�������ᱵ���ֳ������ɣ�ԭ��Һ���������Ʋ��ֱ���������D��ȷ��
���������ᷴӦ�ų�������̼����B������̼�������Һ�ų�������������ʹʪ���ʯ����ֽ����������֤��̼��������Һ�ʼ��ԣ���C ��������õ�����������Һ�м����������Ȼ�����Һ�����ְ�ɫ�������ټ���ϡ���ᣬ���������ܽ⣬˵�������ᱵ�������ᱵ���ֳ������ɣ�ԭ��Һ���������Ʋ��ֱ���������D��ȷ��

����Ŀ��̽��Mg(OH)2���ܽ�ƽ��ʱ�������±������Լ��������飬����˵���в���ȷ����
��� | �� | �� | �� |
��ɢ�� | Mg(OH)2 | HCl | NH4Cl |
��ע | ����Һ | 1 mol/L | 1 mol/L |
A. ����е��뼸�η�̪��Һ����Һ�Ժ�ɫ˵��Mg(OH)2��һ���������
B. Ϊ��ʹMg(OH)2����Һ�ܽ�ø��죬���������NH4ClŨ��Һ�������Ч������
C. �����ۻ�Ϻ�����Ӧ��Mg(OH)2(s)+2NH4+(aq)![]() Mg2+(aq)+2NH3��H2O(aq)
Mg2+(aq)+2NH3��H2O(aq)
D. ����м������H+��OH����Ӧ����H2O��ʹc(OH��)��С��Mg(OH)2�ܽ�ƽ�����ܽⷽ���ƶ�
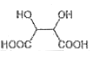
����Ŀ��ij�о���ѧϰС��Ϊ��̽������ĵ������,����������ʵ�顣��pH�Ʋⶨ25 ��ʱ��ͬŨ�ȵĴ����pH���������£�
����Ũ��/mol��L��1 | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
��1��д������ĵ��뷽��ʽ��__________________________��
��2�����ݱ������ݣ����Եó�������������ʵĽ��ۣ�����Ϊ�ó��˽��۵�������__________________��
��3���������Һ�м���һ������NaOH��Һ���������Һ��pH=7ʱ����Һ�����ӵ�Ũ�ȴ�СΪ____
��4��25������0.1mol/L��CH3COOH��Һ��0.1mol/L��NaOH��Һ�������Ϻ���Һ��pH=10����û����Һ����ˮ�������c(OH-)=___________mol/L��д���û����Һ��������ʽ�ľ�ȷ���(���������Ƽ���)��c(Na��)��c(CH3COO��)��______________mol/L��
��5�����з����У�����ʹ0.10 mol��L��1 CH3COOH�ĵ���̶��������___________
a����������0.10 mol��L��1��ϡ���� b������CH3COOH��Һ
c����ˮϡ����0.010 mol��L��1 d����������������
e����������þ�� f����������0.10 mol��L��1��NaOH��Һ
��6������ʱ����ĵ��볣��Ka=1.8��10-5 ����CH3COO����ˮ�ⳣ��Kh= ____________