题目内容
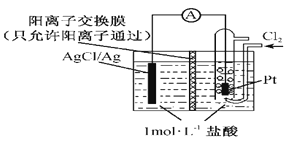
【题目】利用如图所示装置可制取 H2,两个电极均为惰性电极,c 为阴离子交换膜。下列叙述正确的是

A. a 为电源的正极
B. 工作时,OH向左室迁移
C. 右室电极反应为:C2H5OH+H2O4e=CH3COO+5H+
D. 生成 H2 和 CH3COONa 的物质的量之比为 2:1
【答案】D
【解析】A. 根据图示,电解池只左侧生成氢气,是溶液中的水放电,发生了还原反应,左侧电极为阴极,则a 为电源的负极,故A错误;B. 工作时,阴极水放电生成氢气和氢氧根离子,氢氧根离子浓度增大,向右室迁移,故B错误;C. 右室电极为阳极,发生氧化反应,根据图示,右侧溶液显碱性,不可能生成氢离子,故C错误;D. 根据得失电子守恒,生成1mol H2转移2mol电子,则生成 CH3COONa 的物质的量为![]() =0.5mol, H2 和 CH3COONa 的物质的量之比为2:1,故D正确;故选D。
=0.5mol, H2 和 CH3COONa 的物质的量之比为2:1,故D正确;故选D。

练习册系列答案
相关题目