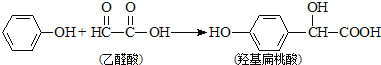题目内容
【题目】向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol<n(CO2) ![]() 0.015mol时发生的反应是:
0.015mol时发生的反应是:
2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
A. A B. B C. C D. D
【答案】D
【解析】试题分析:向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,首先氢氧化钠和二氧化碳反应生成碳酸钠和水,0.02mol氢氧化钠消耗0.01mol二氧化碳,生成0.01mol碳酸钠;之后偏铝酸钠和二氧化碳反应生成氢氧化铝和碳酸钠,0.01mol偏铝酸钠消耗0.005mol二氧化碳,生成0.005mol碳酸钠;最后二氧化碳和碳酸钠反应生成碳酸氢钠,消耗0.015mol二氧化碳,生成0.03mol碳酸氢钠。A.未通入二氧化碳时,根据溶液中的电荷守恒有c(Na+)+ c(H+)=c(AlO2-)+c(OH-),c(Na+)<c(AlO2-)+c(OH-),故A错误;B.当通入的二氧化碳为0.01mol时,则溶液为含有0.01mol碳酸钠和0.01mol偏铝酸钠的混合液,因为HCO3- > Al(OH)3,所以水解程度CO32-< AlO2-,因此c(CO32-) >c(AlO2-),故B错误;C.形成碳酸钠溶液, ![]() +H2O
+H2O![]()
![]() +OH-,H2O
+OH-,H2O ![]() H++OH-,离子浓度的关系为c(Na+)> c(CO32-) > c(OH-)> c(HCO3-),故C错误;D.形成碳酸氢钠溶液,
H++OH-,离子浓度的关系为c(Na+)> c(CO32-) > c(OH-)> c(HCO3-),故C错误;D.形成碳酸氢钠溶液, ![]() + H2O
+ H2O![]() H2CO3 + OH-,溶液显碱性,离子浓度关系为c(Na+)> c(HCO3-)> c(OH-)>c(H+),故D正确。故选D。
H2CO3 + OH-,溶液显碱性,离子浓度关系为c(Na+)> c(HCO3-)> c(OH-)>c(H+),故D正确。故选D。

 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】工业上可用软锰矿浆(主要成分为MnO2)吸收硫酸厂的废气SO2,并制备
MnSO4·H2O晶体,其工艺流程如下:

已知:①浸出液的pH<2,其中的金属阳离子主要是Mn2+,还有少量Fe2+、Al3+等。
②几种离子沉淀时数据信息如下:
离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ |
开始沉淀时pH | 7.6 | 2.7 | 3.8 | 8.3 |
完全沉淀时pH | 9.7 | 4.0 | 4.7 | 9.8 |
请回答下列问题:
(1)加入MnO2氧化时溶液中反应的离子方程式为_______________________________。
(2) 若流程中取消“加入MnO2”,对上述流程的影响是____________________________。
(3)试剂X能否选用碳酸锰(MnCO3)或氢氧化锰[Mn(OH)2],判断并说明理由: ________。
(4)滤渣的主要成分是________,利用滤渣能提取铁红,其原理是___________________。
(5)从滤液中提取MnSO4·H2O晶体的操作是___________________。