题目内容
11.甲、乙、丙三位同学分别用如下实验装置及化学药品[碱石灰(氢氧化钠和生石灰的混合物)]制取氨气.请你参与探究,并回答问题: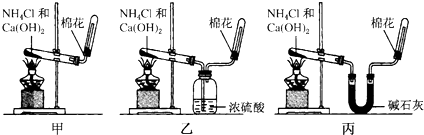
(1)他们制取氨气的化学方程式为:2NH4Cl+Ca(OH)2△_△––––––CaCl2+2H2O+2NH3↑.
(2)三位同学都用向下排空气法收集氨气,其原因是氨气的密度比空气小.
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是乙填(“甲”、“乙”或“丙”).
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的是丙(填“甲”、“乙”或“丙”).
分析 (1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气;
(2)根据氨气的溶解性和密度选择收集氨气的方法;
(3)氨气能与硫酸反应而被硫酸吸收;
(4)碳酸氢铵加热分解生成氨气、二氧化碳和水,可用碱石灰除杂,但不能用NH4HCO3固体代替NH4Cl固体.
解答 解:(1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为2NH4Cl+Ca(OH)2△_△––––––CaCl2+2H2O+2NH3↑,
故答案为:2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O;
(2)氨气易溶于水,不能用排水法收集,氨气密度比空气小,应用向下排空法收集,
故答案为:氨气的密度比空气小;
(3)氨气为碱性气体,通过盛有浓硫酸的洗气瓶时,与硫酸反应而被吸收,故答案为:乙;
(4)碳酸氢铵加热分解生成氨气、二氧化碳和水,其中可用碱石灰吸收二氧化碳和水,只有丙能做到,故答案为:丙.
点评 本题考查氨的实验探究,题目难度中等,注意实验室制备氨气的所用药品.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.在一定条件下,可逆反应N2+3H2?2NH3正反应是放热反应,达到平衡后,当单独改变下列条件时,有关叙述错误的是( )
| A. | 加催化剂,正、逆反应速率都发生变化,且变化的倍数相等 | |
| B. | 加压,正、逆反应速率都增大,且正反应速率增大倍数大于逆反应速率增大倍数 | |
| C. | 降温,正、逆反应速率都减小,且正反应速率减小倍数小于逆反应速率减小倍数 | |
| D. | 加氩气,正逆反应速率都增大,且正反应速率增大倍数大于逆反应速率增大倍数 |
2.下列关于催化剂的说法,正确的是( )
| A. | 催化剂能使不起反应的物质发生反应 | |
| B. | 催化剂在化学反应前后,化学性质和质量都不变 | |
| C. | 催化剂不能改变化学反应速率 | |
| D. | 任何化学反应,都需要催化剂 |
19.已知2Fe3++Cu=Cu2++2Fe2+,现把相同物质的量的硫酸铜、氯化铁和Zn置于水中充分反应后,反应器中所得混合物除含SO42- 和Cl-外,还含有( )
| A. | Zn2+、Cu、Fe3+ | B. | Zn、Cu2+、Fe3+ | ||
| C. | Zn2+、Cu2+、Cu、Fe2+ | D. | Zn2+、Cu2+、Fe、Fe2+ |
6.下列关于二氧化硅的说法中错误的是( )
| A. | 同二氧化碳一样,二氧化硅分子是由一个硅原子和两个氧原子构成的 | |
| B. | 通常状况下,二氧化碳为气态,二氧化硅为固体 | |
| C. | SiO2同CO2一样也能与CaO反应生成盐 | |
| D. | SiO2仅用来表示二氧化硅的组成,其基本结构单元为正四面体,不仅存在于二氧化硅晶体中,而且存在于所有硅酸盐矿石中 |
16.下表中各组物质不能实现如图转化的是:( )


| A. | AlCl3 Al Al(OH)3 | B. | AlCl3 Al(OH)3 NaAlO2 | ||
| C. | CO2 NaHCO3 Na2CO3 | D. | CO2 (NH4)2CO3 NH3 |
20.下列各项叙述中,正确的是( )
| A. | C6H5CH2CH2OH与C6H5OH互为同系物 | |
| B. | CH3CHO与CH3COOH在一定条件下均能与新制氢氧化铜反应 | |
| C. |  与 与  互为同分异构体 互为同分异构体 | |
| D. | H2O与D2O互为同素异形体 |
1.设NA表示阿伏伽德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,48g O3含有的氧原子数为3NA | |
| B. | 17g的OH-离子中含有的电子数为0.1NA | |
| C. | 常温常压下,11.2L氧气中所含有的原子数为NA | |
| D. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA |