题目内容
3.在一密闭容器中充入H2和Br2(气)的混合气,发生H2(g)+Br2(g)═2HBr(g)+Q(Q>0),当达到平衡后,改变某一反应条件(混合气体的物质的量不变),容器内气体的压强增大,下列说法正确的是( )| A. | 平衡可能向逆反应方向移动 | B. | 混合气体的密度一定增大 | ||
| C. | 容器内混合气体的颜色变浅 | D. | 正,逆反应速率一定加快 |
分析 该反应为反应前后气体体积不变的放热反应,混合气体的物质的量不变而容器内压强增大,只能是升高了温度,导致气体压强增大.
解答 解:该反应为反应前后气体体积不变的放热反应,混合气体的物质的量不变而容器内压强增大,只能是升高温度,导致气体压强增大,
A、升温平衡逆向移动,故A正确;
B、混合气体质量和体积不变,密度不变,故B错误;
C、升温平衡逆向移动,容器内混合气体的颜色变深,故C错误;
D、升温正逆反应速率增大,故D正确;
故选AD.
点评 本题考查化学反应速率与化学平衡的影响因素,判断改变的条件为升高温度是解题的关键,题目难度中等.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. | 矿泉水中含有多种微量元素,经常饮用有益身体健康 | |
| B. | 营养强化剂吃的越多越好 | |
| C. | 合理选择饮食,正确使用药物是人体健康的保证 | |
| D. | 大部分药物都无毒副作用,都是非处方药 |
11.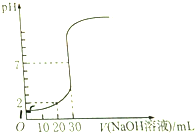 用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )
用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )
 用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )
用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )| A. | 0.12,0.04 | B. | 0.04,0.12 | C. | 0.12,0.06 | D. | 0.03,0.09 |
18.关于同温同压下等体积的NO2和NO的叙述:①质量相等;②密度相等;③所含分子数相等;④所含氮原子个数相等.其中正确的是( )
| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ③ |
1.(1)实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$ TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:

有关物质的性质如下表:
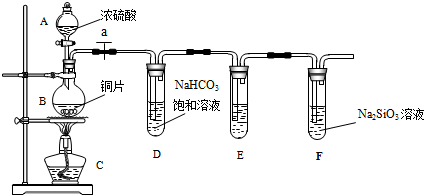
仪器A的名称是干燥管.装置E中的试剂是浓硫酸.反应开始前依次进行如下操作:
组装仪器、检验装置气密性、加装药品,通N2一段时间后点燃酒精灯.反应结束后的操作包括:
①停止通N2②熄灭酒精灯③冷却至室温.正确的顺序为②③①(填序号).欲分离D中的液态混合物,所采用操作的名称是蒸馏.

有关物质的性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
组装仪器、检验装置气密性、加装药品,通N2一段时间后点燃酒精灯.反应结束后的操作包括:
①停止通N2②熄灭酒精灯③冷却至室温.正确的顺序为②③①(填序号).欲分离D中的液态混合物,所采用操作的名称是蒸馏.
5.在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A. | v(A)=0.3mol/(L•s) | B. | v(B)=0.3mol/(L•s) | C. | v(C)=0.3mol/(L•s) | D. | v(D)=1mol/(L•s) |
6.下列做法符合《食品卫生法》的是( )
| A. | 用苏丹红做食品添加剂 | B. | 在奶粉中添加三聚氰胺 | ||
| C. | 用SO2熏制银耳 | D. | 用小苏打发酵面食 |
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: