��Ŀ����
(14��)ij��ȤС��ͬѧ��ʵ�����ü���1-������ŨH2SO4���廯�ƻ����ķ������Ʊ�1-�嶡�飬�����鷴Ӧ�IJ��ָ�����������ͼ��ʾװ�ã����мг�������������������ȴˮ��û�л�����
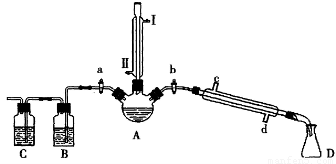
�����ʵ�鲽�裬�ش��������⣺
��1���ر�a��b����ͨ��ֱ�����ܵ�����ˮ����A����30���ӣ��Ʊ�1-�嶡�顣
��ֱ�����ܽ�ͨ����ˮ����ˮ����_____(����I����������)��������������ҪĿ����________��
��2�������ϣ�������Ӧ�ĸ���������У�����(CH3CH2CH2CH2-O-CH2CH2CH2CH3)��1-��ϩ���廯�⡢�������ơ�ˮ�ȡ�Ϩ��ƾ��ƣ�����ֱ�������Ϸ��������Ӳ���a���������ȼ�����Ӧֱ����ȴ��ͨ��B��Cװ�ü��鲿�ָ����
B��C��Ӧʢ�ŵ��Լ��ֱ���_________��????????? ��д��Cװ������Ҫ�Ļ�ѧ����ʽ��___________��
��3��Ϊ�˽�һ�������ᴿ1-�嶡�飬����ȤС��ͬѧ�������л�������������ʾ��
���� | �۵�/�� | �е�/�� |
1-���� | -89��5 | 117��3 |
1-�嶡�� | -112��4 | 101��6 |
���� | -95��3 | 142��4 |
1-��ϩ | -185��3 | -6��5 |
���㲹������ʵ�鲽�裬ֱ�������1-�嶡�顣
������ƿ��ȴ��ȥ��ֱ�������ܣ�
��____����_____����_______����_______���ռ�������֡�
��4����ʵ������ȡ1-������NaBr�ֱ�Ϊ7��4 g��13��0 g�������Ĵֲ��ᆳϴ�ӡ�������ٴ�����õ�9��6 g1-�嶡�飬��1-�嶡��IJ�����_____��������2λ��Ч���֣�
��1����? ��ַ�Ӧ����߷�Ӧ���ת����
��2��̼��������Һ����ˮCH3CH2CH= CH2+Br2��BrCH2CHBrCH2CH3
��3�������ϴ���Ƥ�����¶ȼ�
���ر�a����b
����ͨ�����ܵ�����ˮ��ʹ��ˮ��d������
��Ѹ�������¶���101��6��
��4��70%
��������
�����������1��Ϊ��ʹ����Ч�����ã�Ҫ�����ӽ�ˮ�ڡ������ӳ�ˮ�ڡ�������������ҪĿ���Ǽ��ٷ�Ӧ��1-�����Ļӷ���ʹ��Ӧ���ַ�Ӧ���Ӷ���߷�Ӧ���ת���ʡ���2����������Ӧ�ĸ������ж���(CH3CH2CH2CH2-O-CH2CH2CH2CH3)��1-��ϩ���廯�������壬�����ȶ���ǿ�����������������ʷ�����Ӧ���廯���ˮ��ҺΪHBr������NaHCO3������Ӧ��NaHCO3+2HBr=2NaBr+ CO2 �� + H2O����˿�����NaHCO3����������ڣ�1-��ϩ�Dz�����������������ˮ�����Ը��������Һ��������������ˮ�����飬��Ӧ�ķ���ʽΪ��CH3CH2CH= CH2+Br2��BrCH2CHBrCH2CH3����3�������ʵ�鲽��Ϊ�������ϴ���Ƥ�����¶ȼ�? ���ر�a����b? ����ͨ�����ܵ�����ˮ��ʹ��ˮ��d�����룬��c��������Ѹ�������¶���101��6�����ռ�������ּ�Ϊ1-�嶡�顣��4��n(����)=m/M=7��4 g��74g/mol= 0��1mol? ;n(NaBr)=m/M=13��0 g��103g/mol =0��126mol����Ϊ���߷�����Ӧʱ�����ʵ����ı�Ϊ1:1������NaBr��������ӦӦ�ð��ն��������㡣n(1-�嶡��)=m/M=9��6g��137g/mol=0��07mol������1-�嶡��IJ�����(0��07mol��0��1mol)��100%=70%��
���㣺�����л�����Ʊ���������ļ��顢���ʵIJ��ʵļ��㡣��Ҫ��������װ�õ����ӡ��Լ���ѡ��Ӧ����ʽ����д��ʵ�鲽����Ⱥ�˳��ͷ�Ӧ����IJ��ʵ��йؼ����֪ʶ��

��ش��������⣺
��1����ѡ���Ҫ��װ�ã����������������˳��Ϊ
��2�������������ʵ��װ�ã��������ʵ�鲽�裺��
��3�����ݼ�¼���£�
| ���մɹܵ����� | �մɹ���ص������� | �մɹ������������� |
| 14.80g | 15.19g | 15.47g |
��4���������ؿ����ն�����̼����������������˿�����Ϊ�ɴ���DZͧ���ܱ�ϵͳ��������������д�����������������̼��Ӧ�Ļ�ѧ����ʽ��
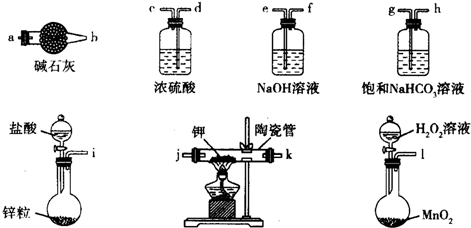
(14��) ij��ȤС��ͬѧ��ʵ�����ü���l��������ŨH2SO4���廯�ƻ����ķ������Ʊ�1���嶡�飬�����鷴Ӧ�IJ��ָ�������������װ�ã����мг�������������������ȴˮ��û�л�����
�����ʵ�鲽�裬�ش��������⣺
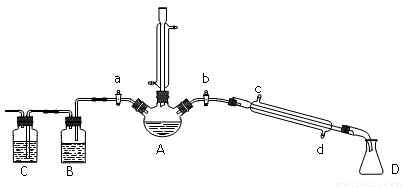
(1) �ر�a��b����ͨ��ֱ�����ܵ�����ˮ����A����30���ӣ��Ʊ�1���嶡�顣��ֱ�����ܵ�������_____________________��
(2) �������ϣ�������Ӧ�ĸ���������У����ѡ�________________����ṹ��ʽ�����廯�⡢�������ơ�ˮ�ȡ�
��Ϩ��ƾ��ƣ�����ֱ�������Ϸ��������ӡ���a���������ȼ�����Ӧֱ����ȴ��ͨ��B��Cװ�ü��鲿�ָ����B��C��Ӧʢ�ŵ��Լ��ֱ���__________��___________
����ͬѧͨ��ij�����������ò����к��С���CH2CH2CH2CH3���� �Ӷ�ȷ���������д��ڶ��ѡ���ͬѧ�Ĺ۵�___________�����ȷ������ԭ����____________
_______________________________________��
(3) Ϊ�˽�һ�����롢�ᴿ1���嶡�飬����ȤС��ͬѧ�������л�����й��������£�
���㲹������ʵ�鲽�裬ֱ�������1���嶡�顣
|
���� |
�۵㣯�� |
�е㣯�� |
|
1�C���� |
�C 89.5 |
117.3 |
|
1�C�嶡�� |
�C 112.4 |
101.6 |
|
���� |
�C 95.3 |
142.4 |
|
1�C��ϩ |
�C 185.3 |
�C 6.5 |
�ٴ���ƿ��ȴ��ȥ��ֱ�������ܣ�
�ڲ��ϴ���Ƥ�����¶ȼƣ�
��______________________��
�ܽ�ͨ�����ܵ�����ˮ��ʹ��ˮ��________�����룻
��Ѹ�������¶���____________���ռ�������֡�
(4) ��ʵ������ȡ1�C������NaBr�ֱ�Ϊ7.4 g��13.0 g��ŨH2SO4�������������Ĵֲ��ᆳϴ�ӡ�������ٴ�����õ�9.6 g 1�C�嶡�飬��1�C�嶡��IJ�����____________��
 ��4�����жϢ���Dװ�����ɹ���ijɷ����Ƶ����λ�����ʽ�Σ��������ּ�Ҫ˵�����ɡ�
��4�����жϢ���Dװ�����ɹ���ijɷ����Ƶ����λ�����ʽ�Σ��������ּ�Ҫ˵�����ɡ�

 ��4�����жϢ���Dװ�����ɹ���ijɷ����Ƶ����λ�����ʽ�Σ��������ּ�Ҫ˵�����ɡ�
��4�����жϢ���Dװ�����ɹ���ijɷ����Ƶ����λ�����ʽ�Σ��������ּ�Ҫ˵�����ɡ�