题目内容
【题目】如表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为 .
(2)表中元素原子半径最大的是(写元素符号) .
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 .
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1mol X的最高价化合物,恢复至室温,放热687kJ.已知该化合物的熔、沸点分别为﹣69℃和58℃.写出该反应的热化学方程式: .
(5)碳与镁生成的1mol化合物Q与水反应生成2mol Mg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为 . Q与水反应的化学方程式为 .
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50,为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2molL﹣1 NaOH溶液和1mol O2 , 则两种气体的分子式及物质的量分别为 , 生成硫酸铜物质的量为 .
【答案】
(1)第三周期ⅤⅡA族
(2)Si
(3)ac
(4)Si(s)+2Cl2(g)=SiCl4(l)△H=﹣687kJ/mol
(5)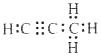 ;Mg4C3+4H2O=3Mg(OH)2↓+C3H4↑
;Mg4C3+4H2O=3Mg(OH)2↓+C3H4↑
(6)NO 0.9mol,NO2 1.3mol;2mol
【解析】(1)Z为Cl元素,其原子序数为17,位于周期表中第三周期、ⅤⅡA族,所以答案是:第三周期ⅤⅡA族;(2)同一周期从左向右,原子半径逐渐减小,同一主族从上到下,原子半径逐渐增大,则原子半径最大的为Si,所以答案是:Si;(3)a.Y单质与H2S溶液反应,溶液变浑浊,说明氧气的氧化性比硫强,则说明Y元素的非金属性比S元素的非金属性强,故a正确;b.在氧化还原反应中,1molY单质比1molS得电子多,氧化性强弱与得失电子数没有必然关系,故b错误;c.元素的非金属性越强,氢化物的稳定性越强,Y和S两元素的简单氢化物受热分解,前者的分解温度高,说明Y的非金属性较强,故c正确;所以答案是:ac;(4)X(Si)与Z(Cl)两元素的单质反应生成1molX的最高价化合物SiCl4 , 恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为﹣69℃和58℃,则常温下SiCl4为液态,该反应的热化学方程式为:Si(s)+2Cl2(g)=SiCl4(l)△H=﹣687kJ/mol,
所以答案是:Si(s)+2Cl2(g)=SiCl4(l)△H=﹣687kJ/mol;(5)该烃分子中碳氢质量比,根据“碳与镁生成的1mol化合物Q与水反应生成2mol Mg(OH)2和1mol烃”可知该烃的化学式为C3H4;Q的化学式为Mg4C3 , Mg4C3与水反应生成氢氧化镁和C3H4。所以答案是: ![]() ;Mg4C3+4H2O=3Mg(OH)2↓+C3H4↑;(6)铜与一定浓度的硝酸和硫酸的混合酸反应可能生成一氧化氮和二氧化氮,相对分子质量都小于50,符合题意,1mol氧气参与反应转移电子的物质的量为4mol,假设二氧化碳的物质的量为x,NO的物质的量为y,
;Mg4C3+4H2O=3Mg(OH)2↓+C3H4↑;(6)铜与一定浓度的硝酸和硫酸的混合酸反应可能生成一氧化氮和二氧化氮,相对分子质量都小于50,符合题意,1mol氧气参与反应转移电子的物质的量为4mol,假设二氧化碳的物质的量为x,NO的物质的量为y,
则: ![]() ,解得:
,解得: ![]() ;根据电子守恒,参与反应的Cu的物质的量为:n(Cu)=
;根据电子守恒,参与反应的Cu的物质的量为:n(Cu)= ![]() =2mol,
=2mol,
所以答案是:NO 0.9mol,NO2 1.3mol;2mol.

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
