题目内容
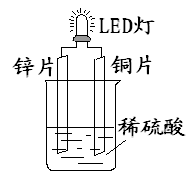
有a、b、c 3种金属,将a、b放在稀硫酸中,用导线连接,电流方向由a到b。把a放在c的硫酸盐溶液中,a表面有c析出。这3种金属的活动性顺序是( )。
| A.b>a>c | B.a>b>c | C.c>b>a | D.c>a>b |
A
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。据此可知a、b相连时,电流方向由a到b,所以b的活泼性强于a的;一般活泼金属置换不活泼金属,所以根据把a放在c的硫酸盐溶液中,a表面有c析出可知,a的金属性强于c的,所以金属性强弱顺序是b>a>c,答案选A。
点评:该题的关键是明确金属性的强弱判断依据,然后结合题意灵活运用即可,有利于培养学生的逻辑推理能力和发散思维能力,有助于提升学生的学科素养,提高学生的学习效率。

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目