题目内容
【题目】(1)基态Fe原子的简化电子排布式为______________________。
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式______________;Fe(CO)5分子中σ键与π键之比为______________。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是_____________;(SCN)2分子中硫原子的杂化方式是_____________;
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是_________________。
②与NH3互为等电子体的一种阴离子为_____________(填化学式);氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因__________。
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为________________。
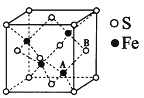
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为___________________;A原子距离B原子所在立方体侧面的最短距离为________________pm(用x表示); 该晶胞的密度为____________g·cm-3。(阿伏加德罗常数用NA表示)
【答案】[Ar] 3d64s2 ![]() 1:1 N sp3杂化 平面三角形 CH3- NH3通过氢键形成“缔合”分子,分子间作用力增强,分子间距离减小,导致密度反常增大。 12 FeS 0.25x
1:1 N sp3杂化 平面三角形 CH3- NH3通过氢键形成“缔合”分子,分子间作用力增强,分子间距离减小,导致密度反常增大。 12 FeS 0.25x ![]()
【解析】
(1)铁元素位于周期表中第四周期第Ⅷ族,原子序数是26,其基态原子的简化电子排布式为[Ar]3d64s2;
(2)CO分子中C与O原子形成了三键,其电子式为:![]() ;Fe(CO)5是由CO和Fe形成的羰基配合物,所以分子中σ键总数为10,π键总数为10,所以二者个数比例为1:1;
;Fe(CO)5是由CO和Fe形成的羰基配合物,所以分子中σ键总数为10,π键总数为10,所以二者个数比例为1:1;
(3)周期表中从左至右,第一电离能呈现增大趋势,从下至上第一电离能呈现增大趋势,此外,相同周期ⅡA第一电离能大于ⅢA的,ⅤA第一电离能大于ⅥA的,所以Ni(SCN)2中N元素的第一电离能最大;(SCN)2的结构为![]() ,S原子形成2个成键电子对以及2个孤电子对,总计4个价层电子对,所以S原子采用的是sp3的杂化方式;
,S原子形成2个成键电子对以及2个孤电子对,总计4个价层电子对,所以S原子采用的是sp3的杂化方式;
(4)①![]() 中有3个成键电子对,经过计算不含孤电子对,所以
中有3个成键电子对,经过计算不含孤电子对,所以![]() 是平面三角形;
是平面三角形;
②书写与NH3互为等电子体且为阴离子的粒子时,可以考虑用族序数比N元素小的其他元素代替N元素,如C,所以可以为![]() ;氨分子之间可以形成氢键,因此可能会通过氢键形成缔合分子,分子间作用力增强,分子间间距减小,进而导致密度比理论密度大;
;氨分子之间可以形成氢键,因此可能会通过氢键形成缔合分子,分子间作用力增强,分子间间距减小,进而导致密度比理论密度大;
(5)单质铜采用的是面心立方最密堆积,Al与Cu采用相同的堆积方式,所以Al的配位数也是12;
(6)由晶胞的结构可知,Fe存在于晶胞的内部,一共有4个,S存在于晶胞的顶点和面心上,所以均摊法计算一个晶胞有4个S原子,晶胞中Fe与S的个数比为1:1,所以该物质的化学式为FeS;由FeS的晶胞结构可知,其与ZnS具有相似的晶胞结构,将晶胞八等分,那么A原子则位于下层四个小正方体中右侧的正方体的体心,所以与B原子所在平面的距离即晶胞边长的![]() ,即0.25xpm;根据晶胞结构,列式计算,晶胞的密度为:
,即0.25xpm;根据晶胞结构,列式计算,晶胞的密度为: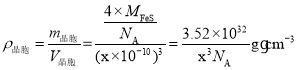 。
。