题目内容
某实验小组为确定过氧化氢分解的最佳催化条件,用如图实验装置进行实验,反应物用量和反应停止的时间数据如下:
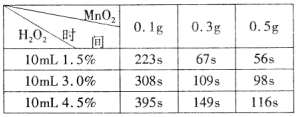
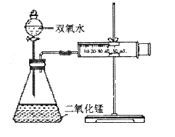
分析表中数据回答下列问题,
(1)相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加而____________。
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入_____g的二氧化锰为较佳选择。
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确_______理由是_________________。


分析表中数据回答下列问题,
(1)相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加而____________。
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入_____g的二氧化锰为较佳选择。
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确_______理由是_________________。
(1)加快(2)0.3(3)不正确 从表中数据可知:相同体积3.0℅的双氧水中溶质的含量是1.5℅的双氧水中溶质的含量的2倍,但反应时间却比其反应时间的2倍要小很多。由反应速率计算公式(ΔV=ΔC∕Δt)可得出:此实验条件下双氧水的浓度越大,分解速率越快。
试题分析:(1)根据表中每一行的数据可看出:相同浓度的过氧化氢中二氧化锰用量越多,反应需要的时间就越短。分解速率越快。即相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加加快。(2)由表中的第2、3、4列可看出,二氧化锰用量从0.1g增加到0.3g时,速率增加很多,而当二氧化锰用量从0.3g增加到0.5g时,速率增加无几。故从“绿色化学”的角度考虑在双氧水的浓度相同时加入0.3g的二氧化锰为较佳选择。(3)这种说法是错误的。不能直接看数据的结论。因为根据表中的数据可知:在相同体积3.0℅的双氧水中溶质的含量是1.5℅的双氧水中溶质的含量的2倍,但反应时间却比其反应时间的2倍要小很多。由反应速率计算公式(ΔV=ΔC∕Δt)可得出:在此实验条件下双氧水的浓度越大,分解速率越快,所用时间就越少。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
 CH3OH(g)。
CH3OH(g)。

 增大的措施有 。
增大的措施有 。

 mC(g)+ nD(g);△H<0,下列说法正确的是
mC(g)+ nD(g);△H<0,下列说法正确的是
 2 SO3的叙述错误的是
2 SO3的叙述错误的是