题目内容
某探究小组用测量HNO3与大理石反应过程中因二氧化碳逸出质量减小的方法,研究影响反应速率的因素。限选试剂:(实验过程中不考虑稀硝酸的挥发)
1.0mol·L-1 HNO3、2.0mol·L-1 HNO3、细颗粒大理石、粗颗粒大理石、35 ℃水浴
(1)请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
以上表格中实验①、③、④空格处应填 、 、 。
(2)整个实验中应控制的不变量是硝酸溶液体积和 。
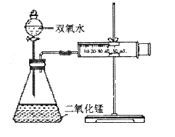
(3)该实验小组用如图实验装置进行实验。
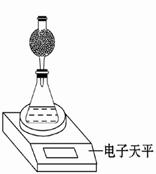
①除电子天平、干燥管、胶头滴管、秒表、玻璃棒、锥形瓶、药匙、胶塞等仪器外,必需的玻璃仪器还有 。
②干燥管中应放置的试剂是 。
A.碱石灰 B.无水CaCl2固体
C.生石灰 D.浓硫酸
③若撤除干燥管装置,所测速率 (填“偏大”、“偏小”或“不变”)。
1.0mol·L-1 HNO3、2.0mol·L-1 HNO3、细颗粒大理石、粗颗粒大理石、35 ℃水浴
(1)请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol·L-1 |
| ① | 常温 | 粗颗粒大理石 | |
| ② | 常温 | 粗颗粒大理石 | 2.0 |
| ③ | | 粗颗粒大理石 | 2.0 |
| ④ | 常温 | | 2.0 |
以上表格中实验①、③、④空格处应填 、 、 。
(2)整个实验中应控制的不变量是硝酸溶液体积和 。
(3)该实验小组用如图实验装置进行实验。

①除电子天平、干燥管、胶头滴管、秒表、玻璃棒、锥形瓶、药匙、胶塞等仪器外,必需的玻璃仪器还有 。
②干燥管中应放置的试剂是 。
A.碱石灰 B.无水CaCl2固体
C.生石灰 D.浓硫酸
③若撤除干燥管装置,所测速率 (填“偏大”、“偏小”或“不变”)。
(1)1.0、35 ℃水浴、细颗粒大理石(各空1分)
(2)大理石的质量(2分)
(3) ①量筒 ②B ③偏大(各空2分)
(2)大理石的质量(2分)
(3) ①量筒 ②B ③偏大(各空2分)
试题分析:(1)影响化学反应速率的因素:温度,浓度,压强,催化剂,反应物的表面积。题中给出了3个变量,要想测得每个变量对化学反应速率的影响,应先控制其他两个变量不变,观察第三个变量对化学反应速率的影响。所以①测的是浓度对化学反应速率的影响。③测的是温度对化学反应速率的影响、④测的是反应物的表面积对化学反应速率的影响。
(2)大理石的质量
(3)①量筒 ②因为此实验采用“测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素”, 质量减小的为二氧化碳的质量。因为干燥管也在电子天平上,质量也计入称量结果,为了测得二氧化碳损失的质量,则干燥管中不可含有吸收二氧化碳的碱石灰。同时为减少二氧化碳逸出所带走的水蒸气造成的实验误差,采用无水CaCl2 、P2O5固体做干燥剂,另外干燥管中不可盛放液体,故D项浓硫酸不选。因为取消干燥管,则二氧化碳逸出所带走的水蒸气造成实验误差,使得减少的质量=m二氧化碳+m水。③使得所测速率偏大。

练习册系列答案
相关题目
 2CO(g) ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是 ( )
2CO(g) ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是 ( )