��Ŀ����
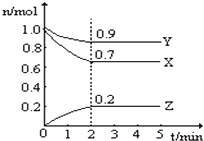
����Ŀ�����ݻ�Ϊ2L���ܱ������н������·�Ӧ��A��g��+2B��g��3C��g��+nD��g������ʼʱAΪ4mol��BΪ6mol��5minĩʱ���C�����ʵ���Ϊ6mol����D��ʾ�Ļ�ѧ��Ӧ����v��D��Ϊ0.4mol/��Lmin������ش������й����⣺
��1��5minĩA�����ʵ���Ũ��Ϊ ��
��2��ǰ5min����B��ʾ�Ļ�ѧ��Ӧ����v��B��Ϊ ��
��3����ѧ����ʽ��nֵΪ ��
��4���˷�Ӧ�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ�� ��v��A ��=5mol/�� Lmin �� ��v�� B ��=6mol/�� Lmin ��
��v��C��=4.5mol/�� Lmin �� ��v��D ��=8mol/�� Lmin ��
���з�Ӧ���������������ţ���
���𰸡�
��1��1mol/L
��2��0.4mol/��L?min��
��3��2
��4����
���������⣺5minĩʱ���C�����ʵ���Ϊ6mol��v��C��= ![]() =0.6mol/��Lmin������D��ʾ�Ļ�ѧ��Ӧ����v��D��Ϊ0.4mol/��Lmin����������֮�ȵ��ڻ�ѧ������֮�ȿ�֪��
=0.6mol/��Lmin������D��ʾ�Ļ�ѧ��Ӧ����v��D��Ϊ0.4mol/��Lmin����������֮�ȵ��ڻ�ѧ������֮�ȿ�֪�� ![]() �����x=2����
�����x=2����
A��g��+ | 2B��g�� | 3C��g��+ | 2D��g�� | |
��ʼ | 4 | 6 | 0 | 0 |
ת�� | 2 | 4 | 6 | 4 |
ƽ�� | 2 | 2 | 6 | 4 |
����1��5minĩA�����ʵ���Ũ��Ϊ ![]() =1mo1/L�����Դ��ǣ�1mol/L�� ��2��ǰ5min����B��ʾ�Ļ�ѧ��Ӧ����v��B��Ϊ
=1mo1/L�����Դ��ǣ�1mol/L�� ��2��ǰ5min����B��ʾ�Ļ�ѧ��Ӧ����v��B��Ϊ ![]() =0.4mol/�� Lmin �������Դ��ǣ�0.4mol/�� Lmin ������3��������������֪��n=2�����Դ��ǣ�2����4����Ӧ�����뻯ѧ�������ı�ֵԽ��Ӧ����Խ�죬�����
=0.4mol/�� Lmin �������Դ��ǣ�0.4mol/�� Lmin ������3��������������֪��n=2�����Դ��ǣ�2����4����Ӧ�����뻯ѧ�������ı�ֵԽ��Ӧ����Խ�죬����� ![]() =5������
=5������ ![]() =3������
=3������ ![]() =1.5������
=1.5������ ![]() =4����Ȼ���б�ֵ���Ӧ������죬���Դ��ǣ��٣�
=4����Ȼ���б�ֵ���Ӧ������죬���Դ��ǣ��٣�
�����㾫����������Ҫ�����˻�ѧƽ��ļ�������֪ʶ�㣬��Ҫ���շ�Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%������ȷ�����⣮

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��ͨ��ʵ�顢�۲졢��ȡ������ȷ����ó���ȷ�Ľ����ǻ�ѧѧϰ�ķ���֮һ�������з�Ӧ���ƶϻ������ȷ������������
ѡ�� | ���� | ���ܵ�ʵ������ | ���� |
A | ij��Һ�м��������ữ���Ȼ�����Һ | �а�ɫ�������� | ��Һ��һ������SO |
B | ��SO2ͨ��Ba(NO3)2��Һ�� | �а�ɫ�������� | SO2��Ba(NO3)2��Ӧ ����BaSO3 |
C | ͬ��ͬѹ�£���pH��ֽ�ⶨ��ͬŨ�ȵ�̼���ƺ���������Һ������� | ̼������Һ��pH������������Һ��pH | ̼������Һ������ˮ�� |
D | �����KI��Һ��ͨ��Cl2 | ��Һ���� | Cl2����۷�����ɫ��Ӧ |
A. A B. B C. C D. D