题目内容
17.下列反应的离子方程式书写正确的是( )| A. | 二氧化硫通入溴水使其褪色 SO2+Br2+2H2O═4H++2Br-+SO32- | |
| B. | 氯化铝溶液中加入过量的氨水 Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| C. | 小苏打溶液中滴加醋酸溶液 HCO3-+CH3COOH=CH3COO-+H2O+CO2↑ | |
| D. | 明矾溶液加热水解生成沉淀 Al3++3H2O?Al(OH)3↓+3H+ |
分析 A.二者发生氧化还原反应生成硫酸和氢溴酸;
B.不符合反应客观事实;
C.小苏打溶液中滴加醋酸溶液,反应生成醋酸钠和水、二氧化碳;
D.水解生成沉淀少量,不标注沉淀符号.
解答 解:A.二氧化硫通入溴水使其褪色,离子方程式:SO2+Br2+2H2O═4H++2Br-+SO42-,故A错误;
B.氯化铝溶液中加入过量的氨水,离子方程式:Al3++3 NH3•H2O═Al(OH)3+3NH4+,故B错误;
C.小苏打溶液中滴加醋酸溶液,反应生成醋酸钠和水、二氧化碳,离子方程式:HCO3-+CH3COOH=CH3COO-+H2O+CO2↑,故C正确;
D.明矾溶液加热水解生成氢氧化铝,离子方程式:Al3++3H2O?Al(OH)3+3H+,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,为高考高频考点,注意把握物质的性质以及离子方程式的书写方法,难度不大,注意盐类水解规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.短周期元素甲、乙、丙、丁的原子半径依次增大,其氢化物中甲、乙、丙、丁的化合价如表所示.下列说法中正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 化合价 | -2 | -3 | -4 | -2 |
| A. | 元素非金属性:甲<乙 | B. | 含氧酸的酸性:乙<丁 | ||
| C. | 氢化物的沸点:甲>丁 | D. | 丙所形成的单质可能互为同位素 |
12.有关表格中的分类正确的是( )
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 水玻璃 | 盐酸 | 硫酸 | 次氯酸 | 干冰 |
| B | 冰 | 氨水 | 碳酸钙 | 水 | 氨气 |
| C | 氯水 | 漂白粉 | 苛性钠 | 碳酸 | 氯化银 |
| D | 苏打 | 赤铁矿 | 氯化钡 | 氢硫酸 | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
2.某温度下,饱和KCl溶液的密度为1.17g•cm-3,其中KCl的质量分数为25.4%,则该温度下,KCl的溶解度为( )
| A. | 46.0 g | B. | 34.0 g | C. | 25.4 g | D. | 21.7 g |
6.下列离子方程式书写正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸钙和醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| C. | 锌和硝酸银溶液反应:Zn+Ag+═Zn2++Ag | |
| D. | 氧化铜与稀盐酸反应:CuO+H+═Cu2++H2O |
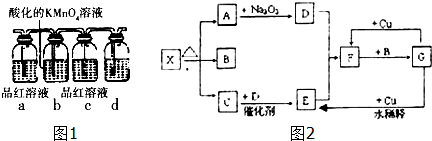
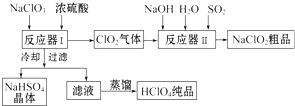 工业上生产高氯酸时,还同时生产一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),工艺流程如下:
工业上生产高氯酸时,还同时生产一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),工艺流程如下: