题目内容
18.设NA为阿伏伽德罗常数,下列说法正确的是( )| A. | 常温下,78gNa2O2与足量的水反应转移电子数为2NA | |
| B. | 常温常压下,8g O3所含电子数为4NA | |
| C. | 0.1mol/L的Na2CO3溶液中所含Na+数目为0.2NA | |
| D. | 标准状况下,22.4L CCl4含CCl4分子数为NA |
分析 A.过氧化钠中氧元素的化合价为-1价,1mol Na2O2与水完全反应生成0.5mol氧气,转移了1mol电子;
B.1个臭氧分子含有24个电子;
C.溶液的体积未知;
D.气体摩尔体积适用对象为气体.
解答 解:A.78gNa2O2的物质的量为1mol,与水完全反应生成0.5mol氧气,转移了1mol电子,转移电子数为NA,故A错误;
B.1个臭氧分子含有24个电子,8g臭氧物质的量为$\frac{8g}{48g/mol}$=$\frac{1}{6}$mol,含电子的个数为$\frac{1}{6}$×24×NA=4NA,故B正确;
C.溶液的体积未知,无法计算碳酸钠的物质的量,故C错误;
D.标况下,四氯化碳为液体,不能使用气体摩尔体积,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意气体摩尔体积的使用对象.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
8.能用于鉴别SO2和CO2的溶液是( )
| A. | 澄清石灰水 | B. | 氯化钡溶液 | C. | 品红溶液 | D. | 紫色石蕊试液 |
6.下列物质含有丰富维生素C的是( )
| A. | 牛肉 | B. | 芹菜 | C. | 鸡蛋 | D. | 牛奶 |
13.环境污染已成为人类社会面临的重大威胁,各种污染数不胜数.下列名词与环境污染相关的是( )
①温室效应 ②赤潮 ③潮汐 ④酸雨 ⑤水华 ⑥水俣病 ⑦大脖子病.
①温室效应 ②赤潮 ③潮汐 ④酸雨 ⑤水华 ⑥水俣病 ⑦大脖子病.
| A. | ①②④⑥ | B. | ③⑤⑦ | C. | ①②④⑤⑥ | D. | ②③④⑤⑦ |
3.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| B. | 元素X的一种单质是自然界中硬度最大的物质 | |
| C. | 元素Y的单质只能与盐酸等酸反应生成氢气,而不能和碱反应 | |
| D. | 元素Z可与元素X形成共价化合物XZ2 |
10.某学生配制一定物质的量浓度的氢氧化钠溶液,其中不会使溶液浓度偏低的是( )
| A. | 没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 | |
| B. | 容量瓶刚用蒸馏水洗净,没有烘干 | |
| C. | 定容时,加蒸馏水先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 | |
| D. | 定容时仰视刻度线 |
8.从20世纪20年代起,就有人预言可能存在由4个氧原子构成的氧分子O4,但一直没有得到证实,直到意大利一所大学的科学家使用普通氧分子和带正电的氧离子,制造出了新型氧分子.若该氧分子具有空间对称结构,你认为该分子是( )
| A. | 氧元素的一种同位素 | B. | 氧元素的一种同素异形体 | ||
| C. | 一种新的氧化物 | D. | 由离子键构成的 |
9.将0.02mol铜片溶于100mL 9mol/L HNO3中,产生336mL气体(只含NO、NO2).该气体与一定量O2混合后,用足量NaOH(aq)完全吸收,产物是NaNO3,则O2的体积至少为(气体体积均为标准状况)( )
| A. | 672 mL | B. | 560 mL | C. | 224 mL | D. | 112 mL |
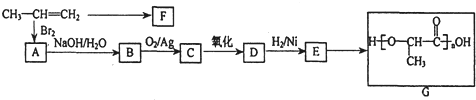
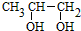 ,D
,D ;
; ;
;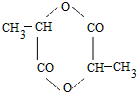 ;
;