题目内容
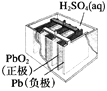
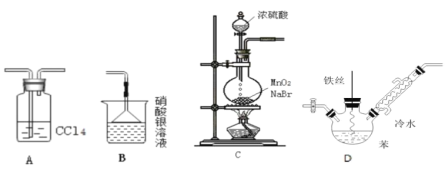
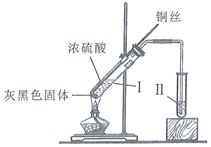
【题目】铜与浓硫酸反应的装置如图所示。下列描述合理的是( )
A.反应过程中,试管Ⅰ中出现灰黑色固体是![]()
B.反应结束后,为观察溶液颜色需向试管Ⅰ中加入水
C.若试管Ⅱ盛放紫色石蕊溶液,可观察到紫色褪至无色
D.为验证气体产物具有还原性,试管Ⅱ可盛放溴水
【答案】D
【解析】
A.铜与浓硫酸反应时可能会发生副反应,生成灰黑色的硫化亚铜,![]() 是红色固体,故A错误;
是红色固体,故A错误;
B.不能直接向试管中加入适量水,浓硫酸剩余时加水放出大量的热可导致液滴飞溅,则取反应后的溶液在烧杯中加水溶解观察颜色,故B错误;
C.铜和浓硫酸在加热的条件下生成了二氧化硫,二氧化硫和水反应会生成亚硫酸,能使紫色石蕊溶液变红,但不褪色,故C错误;
D.实验中产生的二氧化硫气体,通入溴水中,二氧化硫与溴单质和水发生氧化还原反应,生成硫酸和盐酸,会使溴水褪色,溴具有氧化性,二氧化硫体现还原性,故D正确;
答案选D。

练习册系列答案
相关题目
【题目】Ni(CO)4可用于有机合成,也常用作催化剂。一定条件下,一定容积的密闭容器中,发生反应:Ni(s)+4CO(g)![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是
A. 25℃达到平衡时,向容器中继续通入CO,Ni粉转化率增大,CO转化率减小
B. 温度越低,越有利于Ni(CO)4的生产
C. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)<v(逆)
D. 平衡时向密闭容器中加入少量镍粉,平衡向正反应方向移动,新平衡时CO浓度比原平衡小