��Ŀ����
����Ŀ��ij̽��С����HNO3�����ʯ��Ӧ������������С�ķ������о�Ӱ�췴Ӧ���ʵ����ء�����HNO3Ũ��Ϊ1.00 mol��L-1��2.00 mol��L-1������ʯ��ϸ������ֿ������ֹ��ʵ���¶�Ϊ298 K��308 K��ÿ��ʵ��HNO3������Ϊ25.0 mL������ʯ����Ϊ10.00 g��
��1�����������ʵ����Ʊ�������ʵ��Ŀ��һ���������Ӧ��ʵ���ţ�
ʵ���� | T/K | ����ʯ��� | HNO3Ũ��/mol��L-1 | ʵ��Ŀ�� |
�� | 298 | �ֿ��� | 2.00 | ������ʵ��ٺ͢�̽��HNO3Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죻 ������ʵ��ٺ͢�̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죻 ������ʵ��ٺ͢�̽������ʯ��֡�ϸ���Ը÷�Ӧ���ʵ�Ӱ�죻 |
�� | _____ | _____ | _____ | |
�� | _____ | _____ | _____ | |
�� | _____ | _____ | _____ |
��2��ʵ��װ����ͼ1��ʾ����μ����װ�õ�������________________________________

��3��ʵ�����CO2������ʱ��仯�Ĺ�ϵ����ͼ2�����ݷ�Ӧ����ʽCaCO3+2HNO3=Ca(NO3)2+CO2��+H2O������ʵ�����70-90 s��Χ��HNO3��ƽ����Ӧ����________________________
��4�����ڴ���Ŀ�ͼ�У�����ʵ������ۺ͢���CO2������ʱ��仯��ϵ��Ԥ�ڽ��ʾ��ͼ��_______
���𰸡�298�ֿ���1.00308�ֿ���2.00298ϸ����2.00�رշ�Һ©���������������������Ʒ�Һ©���Ļ�������һ��ʱ����ɿ��֣������ֻص�ԭ����λ�ã���֤��װ��������������c(HNO3)=![]() = 1/110=0.009mol��L-1��s-1
= 1/110=0.009mol��L-1��s-1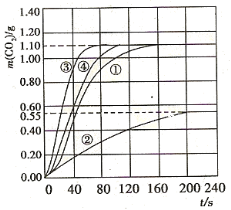
��������
��1����ʵ������ʵ�������Ա�ʵ��̽��Ӱ�췴Ӧ���ʵ����أ���������Ʒ���ʵ��ʱ��Ҫ��Ƴ��ֱ�ֻ��Ũ�ȡ��¶ȺͽӴ������ͬʱ��Ӧ���ʵı仯���Ӷ��ҳ���ͬ������ضԷ�Ӧ���ʵ�Ӱ��������ʵ������ʵ����̽��HNO3Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죬ʵ������ʵ����̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죬��ʵ�������¶�ѡ��308K��ʵ������ʵ����̽���Ӵ�����Ը÷�Ӧ���ʵ�Ӱ�죬��ʵ����ѡ��ϸ�����Ĵ���ʯ��
��2������װ���ص���������Եļ�鷽����
��3����ѧ��Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������ͼ����Լ����70��90s�����ɵ�CO2�������Ȼ����ݷ�Ӧʽ�ɼ�������ĵ���������ʵ������������䷴Ӧ���ʣ�
��4�����ݷ�Ӧ���������������CO2���������������Ӱ�췴Ӧ���ʵ����رȽ�ʵ��ڡ��ۺܷ͢�Ӧ���ʴ�С���Դ��ж�����б�ʴ�С������ͼ��
��1����ʵ��Ŀ�Ŀ�֪��̽��Ũ�ȡ��¶ȡ��Ӵ�����Ի�ѧ��Ӧ���ʵ�Ӱ�죬��ʵ���٢����¶ȡ�����ʯ�����ͬ��ֻ��Ũ�Ȳ�ͬ��ʵ���٢���ֻ���¶Ȳ�ͬ��ʵ���٢���ֻ�д���ʯ���ͬ��
�ʴ�Ϊ�����ϵ��£�������˳����298���ֿ�����1.00��308�� �ֿ�����2.00��298��ϸ������2.00��
��2����װ�õ������Եļ�鷽���ǣ��رշ�Һ©���������������������Ʒ�Һ©���Ļ�������һ��ʱ����ɿ��֣������ֻص�ԭ����λ�ã���֤��װ�����������ã�
��3����70��90s��CO2���ɵ�����Ϊ��m(CO2)=0.95g��0.85g��0.1g��
�ڸ��ݷ���ʽCaCO3+2HNO3=Ca(NO3)2+CO2��+H2O����֪����HNO3�����ʵ���Ϊ��n(HNO3)=![]() ��
��![]() mol��
mol��
����Һ���Ϊ25mL��0.025L������HNO3���ٵ�Ũ�Ȧ�c(HNO3)��![]() =
=![]() mol/L��
mol/L��
�ܷ�Ӧ��ʱ��t��90s��70s��20s
������HNO3��70��90s��Χ�ڵ�ƽ����Ӧ����Ϊ��
v(HNO3)����c(HNO3)/t��![]() =
=![]() mol��L��1��S��1=0.009 mol��L��1��S��1
mol��L��1��S��1=0.009 mol��L��1��S��1
��4��ʵ��ڡ��ۺ͢����ô���ʯ��������Ϊ10.00g�������ʵ���Ϊ![]() =0.1mol��ʵ��١��ۺ͢��������������ͬ��Ϊ��2.00mol/L��0.025L=0.05mol�����ݷ�Ӧ����ʽCaCO3+2HNO3=Ca(NO3)2+CO2��+H2O��֪������㣬����CO2������������������0.05mol
=0.1mol��ʵ��١��ۺ͢��������������ͬ��Ϊ��2.00mol/L��0.025L=0.05mol�����ݷ�Ӧ����ʽCaCO3+2HNO3=Ca(NO3)2+CO2��+H2O��֪������㣬����CO2������������������0.05mol![]() ��44g/mol=1.10g��ʵ��������������Ϊ1.00mol/L��0.025L=0.025mol������ʯ��������Ӧ���ɵ�CO2������Ϊ0.025mol
��44g/mol=1.10g��ʵ��������������Ϊ1.00mol/L��0.025L=0.025mol������ʯ��������Ӧ���ɵ�CO2������Ϊ0.025mol![]() ��44g/mol=0.55g��
��44g/mol=0.55g��
ʵ��ٺ͢�̽��HNO3Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죬��HNO3Ũ�Ȣ�>�ڣ�Ũ��Խ��ӦԽ�죬������б�ʢ�>�ڣ�
ʵ��ٺ͢�̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죬���¶Ȣ۸��ڢ٣��¶�Խ�߷�ӦԽ�죬������б�ʢ�>�٣�
ʵ��ٺ͢�̽������ʯ��֡�ϸ���Ը÷�Ӧ���ʵ�Ӱ�죬��ʵ���Ϊϸ������ʵ���Ϊ�ֿ���������ԽС�������Խ��ӦԽ�죬�ʷ�Ӧ���ʢ�>�٣�������б�ʢ�>�٣�
������������������ͼ�����£�

 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�����Ŀ��������������{[CH3CH(OH)COO]2Fe��3H2O}��һ�ֺܺõ�ʳƷ��ǿ����,������ˮ,����Ч���������ã�����������FeCO3��Ӧ�Ƶ�:
2CH3CH(OH)COOH+FeCO3+2H2O��[CH3CH(OH)COO]2Fe��3H2O +CO2����
I.�Ʊ�̼������:װ����ͼ��ʾ��
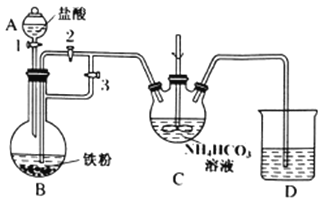
(1)C��������___________��
(2)��ϴ����,���װ��������,A�м�������,B�м�������,C�м���NH4HCO3��Һ��Ϊ˳�����ʵ��Ŀ��,����װ���л����Ĵر�˳��Ϊ:�رջ���______������______���������������,�رջ���1,��Ӧһ��ʱ���,�رջ���____,����_____��C�з����ķ�Ӧ�����ӷ���ʽΪ_______________��
��.�Ʊ�������������:
���Ƶõ�FeCO3����������Һ��,������������,��75���½���ʹ֮��ַ�Ӧ��Ȼ���ټ����������ᡣ
(3)�����������۵�������______________����������Һ�л�������������������ʵ������Ǹ�����������������________�����
��.�����������崿�ȵIJ���:
(4)����KMnO4�ζ����ⶨ��Ʒ��Fe2+�����������㴿��ʱ,���ֽ�����Ǵ���100%,��ԭ�������_____________________��
(5)����������,����Ce(SO4)2����Һ�ζ����вⶨ����Ӧ��Ce4+���ӵĻ�ԭ����ΪCe3+���ⶨʱ,�ȳ�ȡ5.760g��Ʒ,�ܽ����б�Ҫ������������ƿ���Ƴ�250mL��Һ,ÿ��ȡ25.00mL,��0.1000mol/LCe(SO4)2����Һ�ζ����յ�,��¼�������±���
�ζ����� | 0.1000mol/LCe(SO4)2����Һ���/mL | |
�ζ�ǰ���� | �ζ������ | |
1 | 0.10 | 19.85 |
2 | 0.12 | 21.32 |
3 | 1.05 | 20.70 |
���Ʒ��������������Ĵ���Ϊ_________(������������ʾ)��
����Ŀ���屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£�
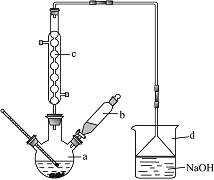
�� | �� | �屽 | |
�ܶ�/g��cm-3 | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
ˮ���ܽ�� | �� | �� | �� |
�����кϳɲ���ش����⣺
��1����a�м���15mL��ˮ����������м����b��С�ļ���4.0mLҺ̬�塣��a�е��뼸���壬�а�ɫ��������������Ϊ������______���塣�÷�ӦΪ_______������ȡ����ȡ�����Ӧ����ȴˮ������_____________����Ͻ��³������½��ϳ������������μ���Һ����ꡣ��������c��������________,�������ǣ�__________________________________��װ��d�������ǣ�_____________________________________________________����ƿ�з������л���Ӧ�ķ���ʽΪ��_______________________________________________��
��2��Һ�����������в�������ᴿ��
����a�м���10mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����Һ������10mLˮ��8mL 10%��NaOH��Һ��10mLˮϴ�ӡ�ϴ�ӡ������л������Լ�����Ҫ�õ��������ǣ�_____________����һ��ˮϴ��ȥ�ֵ�HBr����NaOH��Һϴ�ӵ�������______________���ڶ���ˮϴ��Ŀ���ǣ�____________��ÿһ��ϴ�ӣ��л����_________����¿ڷų������Ͽڵ����������ػ�ɫ���屽�����ᴿ��ָ�Ϊ��ɫ��
����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����ˡ������Ȼ��Ƶ�Ŀ����_____________��
��3�������Ϸ���������屽�л����е���Ҫ���ʱ���Ҫ��һ���ᴿ�����в����б������____��������ȷѡ��ǰ����ĸ����
A�������� B������ �������� C����Һ�� ���� D����ȡ
����Ŀ��ijͬѧ̽������Na��CO2�ķ�Ӧ��ʵ�����£�
ʵ��I | ʵ��II | |
���� | ����ȼ�Ľ������쵽ʢ��CO2�ļ���ƿ�� | ��ʵ��I�ļ���ƿ��ˮ��ϴ�����ˡ�ȡ��ɫ�������գ�ȡ��Һ�ֱ�μӷ�̪���Ȼ�����Һ |
���� | �ٻ���ʻ�ɫ �ڵײ��к�ɫ���壬ƿ���ϸ��а�ɫ���� | �ٺ�ɫ������ȼ ����Һ��ʹ��̪��Һ��죬�μ��Ȼ�����Һ�а�ɫ�������� |
����˵������ȷ����
A. ���ɵĺ�ɫ�����к���CB. ��ɫ������Na2O
C. ʵ��˵��CO2����������D. ����Na�Ż�����CO2���
