题目内容
【题目】H2O2在Fe2+、Cu2+的存在下生成具有强氧化性的OH(羟基自由基),OH可将有机物氧化降解。
(1)Cu2+H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)═CuOOH+(aq)+H+(aq)△H1=a kJmol﹣1
CuOOH+(aq)═Cu+(aq)+OH(aq)+1/2O2(g)△H2=b kJmol﹣1
2CuOOH+(aq)═2Cu+(aq)+H2O2(aq)+O2(g)△H3=c kJmol﹣1
则H2O2(aq)═2OH(aq)△H=_____kJmol﹣1。

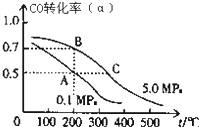
(2)为探究温度对Cu2+H2O2甲基橙去除率的影响,某研究小组在不同温度下进行实验(其他条件相同),实验结果如图所示。相同条件下,温度升高,甲基橙去除速率增大,其原因是_____。
(3)为探究Fe2+Cu2+H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图所示。得出“Fe2+Cu2+H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为_____。
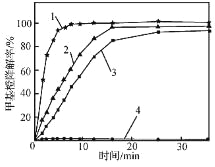
实验条件:200 mL甲基橙模拟废水(1.5 gL﹣1,pH=3.0),温度60℃、V(H2O2)=2.0 mL
1﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0.02:0.4
2﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0.02:0
3﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0:0.4
4﹣V(H2O2):m(FeSO4):m(CuSO4)=2:0:0
(4)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如下图所示。阳极的电极反应式为_____,X微粒的化学式为_____,阴极附近Fe2+参与反应的离子方程式为_____。
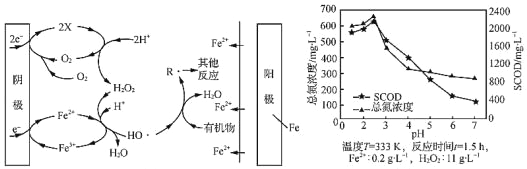
(5)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如上图所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是_____。
【答案】2b﹣c OH浓度增大或活化分子数增多 相同时间时,曲线1对应甲基橙降解率均高于曲线2、曲线3 Fe﹣2e﹣═Fe2+; O2﹣ H2O2+H++Fe2+═Fe3++H2O+OH Fe2+、Fe3+转化为Fe(OH)3
【解析】
(1)由①CuOOH+(aq)═Cu+(aq)+OH(aq)+1/2O2(g)△H2=b kJmol﹣1
②2CuOOH+(aq)═2Cu+(aq)+H2O2(aq)+O2(g)△H3=c kJmol﹣1
结合盖斯定律可知①×2﹣②得到H2O2(aq)═2OH(aq),其△H=(2b﹣c )kJmol﹣1;
(2)图1中相同条件下,温度升高,甲基橙去除速率增大,其原因是OH浓度增大或活化分子数增多;
(3)“Fe2+Cu2+H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为相同时间时,曲线1对应甲基橙降解率均高于曲线2、曲线3;
(4)图3中阳极上Fe失去电子,阳极反应式为Fe﹣2e﹣═Fe2+,阴极上2X+2H+=H2O2+O2,由电荷及元素守恒可知X为O2﹣;阴极附近Fe2+与H2O2反应,结合图中生成物可知离子反应为H2O2+H++Fe2+═Fe3++H2O+OH;
(5)当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是Fe2+、Fe3+转化为Fe(OH)3。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案