题目内容
【题目】(1)用系统命名法对下列有机物进行命名
① _____________________________________________
_____________________________________________
② ____________________________________________
____________________________________________
③写出分子式为C4H8的所有烯烃的结构简式及名称。_______________________________________
(2)下列几种烃类物质:

 环辛四烯
环辛四烯
①正四面体烷的二氯取代产物有________种;立方烷的二氯取代产物有________种。
②关于苯和环辛四烯的说法正确的是________(填字母符号)。
A.都能使酸性KMnO4溶液褪色
B.都能与H2发生加成反应,等质量的苯和环辛四烯消耗H2的物质的量之比为3:4
C.都是碳碳单键和碳碳双键交替结构
D.都能发生氧化反应
③乙烯基乙炔含有的官能团名称是______________________________。
(3)根据下列有机化合物填空。
a.  b.
b. 
①a中所含官能团的名称是_________________________________________________;
②b中所含官能团的结构简式是__________________________________________。
(4)测定实验式:某含C、H、O三种元素的有机物,经燃烧实验测得其碳的质量分数为64.86%,氢的质量分数为13.51%,则其实验式是____。
【答案】2-甲基戊烷 2-甲基-1-丁烯 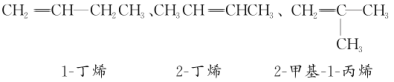 1 3 D 碳碳双键、碳碳三键(或碳碳叁键) 羟基、羧基
1 3 D 碳碳双键、碳碳三键(或碳碳叁键) 羟基、羧基 ![]() 、
、![]() 、—OH C4H10O
、—OH C4H10O
【解析】
(1)烷烃中以含碳最多的碳为主碳链,支链在主链上位次最小;不饱和烃中,以含有碳碳双键在内的最长碳链为主碳链,支链位次最小进行命名;据以上分析解答。
(2)①根据正四面体烷二氯代物的种类取决于一氯代物中氢原子的种类;立方烷的二氯代物取决于一氯代物中氢原子的种类;
②苯不含碳碳双键,性质较为稳定,与高锰酸钾不反应,环辛四烯含有碳碳双键,具有烯烃的性质;
③根据乙烯基乙炔结构简式写出含有的官能团名称;
(3)①根据a的结构简式写出a中所含官能团名称;
②根据b的结构简式写出b中所含官能团结构简式;
(4)根据有机物的元素组成可求出氧元素的质量分数,然后计算出分子中C、H、O三种元素的个数比,进而求出其实验式。
(1)①该烃为烷烃,主碳链为5,为戊烷,2位碳上有1个甲基,因此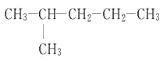 名称为:2-甲基戊烷;综上所述,本题答案是:2-甲基戊烷。
名称为:2-甲基戊烷;综上所述,本题答案是:2-甲基戊烷。
②该烃为烯烃,包含双键在内的主碳链为4,双键在1位碳上,2位碳上有1个甲基,因此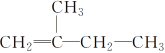 名称为:2-甲基-1-丁烯;综上所述,本题答案是:2-甲基-1-丁烯。
名称为:2-甲基-1-丁烯;综上所述,本题答案是:2-甲基-1-丁烯。
③烯烃含有碳碳双键,分子式为C4H8的所有烯烃的结构简式及名称分别为:
CH2=CH-CH2CH3 ,名称为1-丁烯;CH3CH=CHCH3,名称为2-丁烯;CH2=C(CH3)2,名称为2-甲基-丙烯;综上所述,本题答案是:CH2=CH-CH2CH3 1-丁烯 ,CH3CH=CHCH3,2-丁烯CH2=C(CH3)2 2-甲基-1-丙烯。
(2)①正四面体烷完全对称,只有一种氢原子,一氯代物只有1种,一氯代物中氢原子也只有1种,所以故二氯代物只有1种;立方烷分子中只有一种氢原子,其一氯代物有1种,而一氯代物有3种氢原子,分别在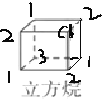 ,则立方烷的二氯代物有3种;综上所述,本题答案是:1;3。
,则立方烷的二氯代物有3种;综上所述,本题答案是:1;3。
②A.苯性质稳定,与酸性KMnO4溶液不反应,故A错误;
B.最简式相同,都能与氢气发生加成反应,等质量的苯和环辛四烯消耗氢气的物质的量之比为1:1,故B错误;
C.苯不是碳碳单键和碳碳双键交替结构,故C错误;
D.两种有机物都可燃烧,都能发生氧化反应,故D正确。
综上所述,本题选D。
③根据乙烯基乙炔的结构简式可知,含有的官能团是碳碳双键、碳碳三键(或碳碳叁键);综上所述,本题答案是:碳碳双键、碳碳三键(或碳碳叁键)。
(3)①根据a的结构简式可知,a中所含官能团是:羟基、羧基;综上所述,本题答案是:羟基、羧基。
②根据b的结构简式可知,b中所含官能团的结构简式分别是:![]() 、
、![]() 、—OH ;综上所述,本题答案是:
、—OH ;综上所述,本题答案是:![]() 、
、![]() 、—OH 。
、—OH 。
(4)碳的质量分数是64.86%,氢的质量分数是13.51%,氧元素质量分数是1-64.86%-13.51%=21.63%,则该物质中碳、氢、氧原子个数之比=64.86/12:13.51/1:21.63/16=4:10:1,所以其实验式为:C4H10O;综上所述,本题答案是:C4H10O。

【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
NaCl溶于水 |
电解CuCl2溶液 |
CH3COOH在水中电离 |
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D










