题目内容
短周期元素X、Y、Z原子序数依次递增。X、Y、Z的最外层电子数之和为13,Y是所在周期中金属性最强的,X、Z在同一主族。
(1)Z元素在周期表中的位置是 。
(2)Y2ZX3溶液显 性,能证明该溶液中存在水解平衡的事实是 (填序号)。
a.滴入酚酞溶液变红,再加入稀H2SO4红色退去
b.滴入酚酞溶液变红,再加入氯水红色退去
c.滴入酚酞溶液变红,再加入BaCl2溶液产生沉淀且红色退去
(3)化合物Cu2X和Cu2Z可发生如下转化(其中D是纤维素水解的最终产物):
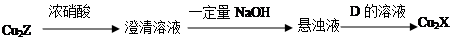
① D的化学式是 ;
② Cu2X与浓硝酸反应有红棕色气体生成,则化学反应方程式是 。
(4)某温度下,在一个5L的密闭容器中充入0.2 mol ZX2和0.1 mol X2,20 s后达到平衡,测得容器中含有0.18 mol ZX3,则用X2表示该反应的平均速率是v(X2) = ,此温度下该反应的化学平衡常数K= 。
(1)Z元素在周期表中的位置是 。
(2)Y2ZX3溶液显 性,能证明该溶液中存在水解平衡的事实是 (填序号)。
a.滴入酚酞溶液变红,再加入稀H2SO4红色退去
b.滴入酚酞溶液变红,再加入氯水红色退去
c.滴入酚酞溶液变红,再加入BaCl2溶液产生沉淀且红色退去
(3)化合物Cu2X和Cu2Z可发生如下转化(其中D是纤维素水解的最终产物):
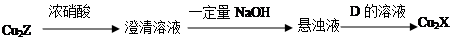
① D的化学式是 ;
② Cu2X与浓硝酸反应有红棕色气体生成,则化学反应方程式是 。
(4)某温度下,在一个5L的密闭容器中充入0.2 mol ZX2和0.1 mol X2,20 s后达到平衡,测得容器中含有0.18 mol ZX3,则用X2表示该反应的平均速率是v(X2) = ,此温度下该反应的化学平衡常数K= 。
26.(14分,每空2分)
(1)第3周期第ⅥA族
(2)碱 C
(3)①C6H12O6 ②Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O
(4)9×10-4 mol/(L·S) 4.05×104 L/mol (不写单位不扣分)
(1)第3周期第ⅥA族
(2)碱 C
(3)①C6H12O6 ②Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O
(4)9×10-4 mol/(L·S) 4.05×104 L/mol (不写单位不扣分)
试题分析:
(1)Z元素是硫元素,在周期表中的位置是第3周期第ⅥA族。Y是所在周期中金属性最强的,Y是钠元素,X是氧元素,
(2)Y2ZX3是Na2SO3溶液,强碱弱酸盐水解溶液呈碱性,当在此溶液中加入BaCl2溶液后,平衡逆向移动,碱性减弱,酚酞颜色变浅。
(3)① D是纤维素水解的最终产物应该是葡萄糖,化学式是C6H12O6 。
② Cu2X与浓硝酸反应有红棕色气体生成,红棕色气体是二氧化氮,说明发生了氧化还原反应,则化学反应方程式是Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O
(4)根据三态法计算模式:2SO2 + O2
 2 SO3
2 SO3开始(mol·L-1) 0.04 0.02 0
转化(mol·L-1) 0.036 0.018 0.036
平衡(mol·L-1) 0.004 0.002 0.036
v(X2) =0.018/20=9×10-4 mol/(L·S) 化学平衡常数K=0.0362/(0.0042 *0.002) = 4.05×104

练习册系列答案
相关题目

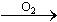 b
b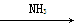
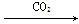 NaHCO3(s)
NaHCO3(s)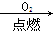 NO2
NO2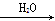 HNO3
HNO3 Mg(OH)2
Mg(OH)2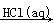 MgCl2(aq)
MgCl2(aq) MgCl2(s)
MgCl2(s)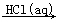 AlCl3(aq)
AlCl3(aq) 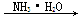 Al(OH)3
Al(OH)3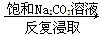 BaCO3
BaCO3 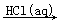 BaCl2(aq)
BaCl2(aq)