题目内容
在2A + B =" 3C" + 4D的反应中,下列表示该反应速率最大的是
A.V(C)=0.5mol / (L·min) B.V(A)=0.8mol / (L·min)
C.V(B)=0.3mol / (L·min) D.V(D)=" 1mol" / (L·min)
B
解析试题分析:首先单位要统一,依据物质的反应速率之比等于其计量数之比,先把不同物质的反应速率换算成同一物质的反应速率进行比较,从而确定选项,对于反应2A+B=3C+4D,都转化为D表示的速率进行比较,A、V(C)=0.5 mol/(L?min),反应速率之比等于其计量数之比,故V(D)=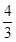 V(C)=0.67mol/(L?min);B、V(A)=0.8mol/(L?min),反应速率之比等于其计量数之比,故V(D)=2V(A)=1.6mol/(L?min);C、V(B)=0.3mol/(L?min),反应速率之比等于其计量数之比,故V(D)=4V(A)=1.2mol/(L?min);D、V(D)=1mol/(L?min),故选:B。
V(C)=0.67mol/(L?min);B、V(A)=0.8mol/(L?min),反应速率之比等于其计量数之比,故V(D)=2V(A)=1.6mol/(L?min);C、V(B)=0.3mol/(L?min),反应速率之比等于其计量数之比,故V(D)=4V(A)=1.2mol/(L?min);D、V(D)=1mol/(L?min),故选:B。
考点:考查学生对化学反应速率及其表示法的理解及应用

 优生乐园系列答案
优生乐园系列答案下列有关化学概念或原理的论述中,正确的是
| A.任何一个氧化还原反应都可以设计为电池,输出电能 |
| B.铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 |
| C.电解饱和食盐水的过程中,水的电离平衡正向移动 |
| D.任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大 |
在一定温度下,容积为2L的密闭容器中x(g).与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若其他条件不变,温度为T1和T2时,Y的体积分数与时间的关系如图(2)所示。下列说法正确的是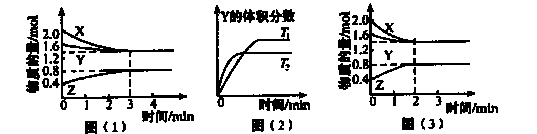
A.容器内发生的反应可以表示为2X(g)+Y(g)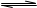 2Z(g) 2Z(g) |
| B.保持其他条件不变,升高温度,该反应的平衡常数K减小 |
| C.反应前3 min内,v(Z)≈0.067 mol·L-1·min-1 |
| D.若改变反应条件,反应进程如图(3)所示,则改变的条件是增大压强 |
一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g) 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
①容器中气体的密度不再发生变化
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成2n mol Z,同时消耗2n mol Y
| A.①② | B.②③ | C.③④ | D.①④ |
下列有关工业生产的叙述正确的是
| A.合成氨工业中,将NH3及时液化分离有利于加快反应速率 |
| B.氯碱工业中,使用离子交换膜可防止C12和NaOH溶液反应 |
| C.硫酸工业中,接触室内安装热交换器,是为了利用沸腾炉中排出的SO2的热量 |
| D.硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响 |
下列有关说法正确的是
| A.反应SiO2(s)+ 3C(s) =" SiC(s)" + 2CO(g)室温下不能自发进行,则该反应的△H<0 |
| B.铅蓄电池放电过程中,正极质量增加,负极质量减小 |
C.25℃下,在NH3·H2O稀溶液中,加水, 的值不变 的值不变 |
| D.在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-水解程度增大,pH增大 |
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是( )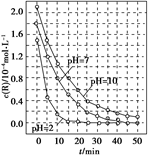
| A.在0-50 min之间, pH = 2和PH = 7时R的降解百分率不相等 |
| B.在 20-25 min之间, pH =" 10" 时R的平均降解速率为0.04 mol?L-1?min-1 |
| C.溶液酸性越强, R 的降解速率越小 |
| D.R的起始浓度和溶液的PH均影响R的降解速率 |
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g)
 Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v(正)>v(逆)
D.80℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g)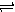 Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
Z(g) △H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是
| A.以Y浓度变化表示的反应速率为0.0005 mol/(L·s) |
| B.其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2 |
| C.其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大 |
| D.其他条件不变,升高温度逆反应速率加快,正反应速率减慢 |